题目内容
14.在下列物质中,不能由两种单质直接通过化合反应制备的是( )| A. | HCl | B. | Na2O | C. | NaCl | D. | FeCl2 |
分析 氯气具有强氧化性,与变价金属反应生成高价金属氯化物,Na与氧气在常温下化合生成氧化钠,以此来解答.
解答 解:A.氢气与氯气化合生成HCl,故A不选;
B.Na与氧气在常温下化合生成氧化钠,故B不选;
C.Na与氯气化合生成NaCl,故C不选;
D.Fe与氯气化合生成FeCl3,故D选;
故选D.
点评 本题考查金属及化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
4.已知金属钠和水反应的化学方程式为:2Na+2H2O═2NaOH+H2↑.将9.2g金属钠投入到足量的重水D2O中,则产生的气体中含有( )
| A. | 0.2 mol中子 | B. | 0.4 mol电子 | C. | 0.2 mol质子 | D. | 0.4 mol分子 |
5.目前银川一中部分学生喜欢使用胶带,四氟乙烯(C2F4)是制作胶带胶黏剂的一种原料.
下面是关于四氟乙烯的几种说法:
①它是由碳、氟两种元素组成的化合物,
②它是由氟气(分子式为:F2)和碳组成的化合物
③它的分子中碳、氟两种元素的原子物质的量比为1:2
这些说法中正确的是( )
下面是关于四氟乙烯的几种说法:
①它是由碳、氟两种元素组成的化合物,
②它是由氟气(分子式为:F2)和碳组成的化合物
③它的分子中碳、氟两种元素的原子物质的量比为1:2
这些说法中正确的是( )
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
2.NA为阿伏加德罗常数,下列分子数最少的是( )
| A. | 标准状况下2.24L氨气 | B. | 0.8mol氧气 | ||
| C. | 3.6g水 | D. | 含NA个氢分子的氢气 |
9.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,2.24L SO3中含有的SO3分子数为0.1NA | |
| B. | 5.6 g Fe与标准状况下2.24L的Cl2充分反应,转移的电子数为0.3NA | |
| C. | 将含3NA个离子的Na2O2固体溶于水配成1L溶液,所得溶液中Na+的浓度为2mol/L | |
| D. | 1molMnO2与4mol浓盐酸充分反应后生成的Cl2分子数为NA |
19.标准状况下,现有①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2molNH3,对这四种气体的氢原子个数由大到小的顺序排列正确的是( )
| A. | ②>③>①>④ | B. | ②>③>④>① | C. | ①>④>②>③ | D. | ①>③>④>② |
6.现有三组溶液,①碘水中提取单质碘 ②碘和四氯化碳的混合物 ③汽油和氯化钠溶液,分离以上混合物的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
13.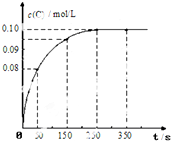 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )| A. | 反应在0~50s的平均速率v(C)=1.6×10-3mol/(L•s) | |
| B. | 该温度下,反应的平衡常数K=0.025 | |
| C. | 保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0 | |
| D. | 反应达平衡后,再向容器中充入 1 mol A,该温度下再达到平衡时0.1mol/L<c(C)<0.2mol/L |
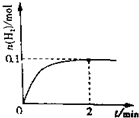 空气中的污染物主要来源为燃煤、机动车尾气等.因此,CO、SO2、NOx等进行研究具有重要意义.请回答下列问题:
空气中的污染物主要来源为燃煤、机动车尾气等.因此,CO、SO2、NOx等进行研究具有重要意义.请回答下列问题: