题目内容
16.下列试剂常用来检验Fe3+的是( )| A. | 氯水 | B. | BaCl2溶液 | C. | KSCN溶液 | D. | KNO3溶液 |
分析 Fe3+遇KSCN溶液变为血红色,作为检验Fe3+的特征试剂,以此来解答.
解答 解:A.氯水与铁离子不反应,不能用于检验,故A错误;
B.氯化钡与铁离子不反应,不能用于检验,故B错误;
C.Fe3+遇KSCN溶液变为血红色,能检验Fe3+,故C正确;
D.KNO3与Fe3+不反应,不能检验,故D错误.
故选C.
点评 本题考查铁离子的检验,为高频考点,侧重于学生的分析能力和实验能力的考查,明确检验的试剂及现象是解答本题的关键,侧重物质性质的考查,题目较简单.

练习册系列答案
相关题目
20.可逆反应A(g)+3B(g)?2C(g)△H=-QkJ/mol.有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同的条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2 kJ;已知Q1=3Q2.下列叙述正确的是( )
| A. | 乙中C的转化率为75% | |
| B. | 反应.达到平衡前,甲中始终有V正>V逆,乙中始终有V正<V逆 | |
| C. | 在该条件下,反应2C(g)?A(g)+3B(g)的平衡常数为2.7×1.54 | |
| D. | 乙中的热化学方程式为2C(g))?A(g)+3B(g)△H=+Q2kJ/mol |
4.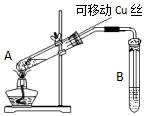 在探究Cu与浓H2SO4反应时,将质量8.0g可移动Cu丝部分伸入浓H2SO4中,充分反应后,Cu丝剩余4.8g,将试管A中液体稀释成100ml溶液.该溶液中Cu2+物质的量浓度约为( )
在探究Cu与浓H2SO4反应时,将质量8.0g可移动Cu丝部分伸入浓H2SO4中,充分反应后,Cu丝剩余4.8g,将试管A中液体稀释成100ml溶液.该溶液中Cu2+物质的量浓度约为( )
 在探究Cu与浓H2SO4反应时,将质量8.0g可移动Cu丝部分伸入浓H2SO4中,充分反应后,Cu丝剩余4.8g,将试管A中液体稀释成100ml溶液.该溶液中Cu2+物质的量浓度约为( )
在探究Cu与浓H2SO4反应时,将质量8.0g可移动Cu丝部分伸入浓H2SO4中,充分反应后,Cu丝剩余4.8g,将试管A中液体稀释成100ml溶液.该溶液中Cu2+物质的量浓度约为( )| A. | 0.25mol•L-1 | B. | 0.5mol•L-1 | C. | 0.025mol•L-1 | D. | 0.05mol•L-1 |
11.一定条件下2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1;CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ•mol-1,则1molCO和3molCH4组成的混合气体在上述条件下完全燃烧放出的热量为( )
| A. | 2912 kJ | B. | 2953 kJ | C. | 3236 kJ | D. | 3836 kJ |
1.常温下,向一定体积的0.1mol/L的醋酸溶液中加水稀释后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目减少 | |
| B. | 醋酸的电离程度增大,c(H+)亦增大 | |
| C. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$不变 | |
| D. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 |
8.在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是( )
| A. | 1:2 | B. | 2:1 | C. | 1:1 | D. | 无法比较 |
5.下列有机物检验方法正确的是( )
| A. | 取少量卤代烃加NaOH水溶液共热,冷却,再加AgNO3溶液检验卤原子存在 | |
| B. | 苯和乙烯都能使溴水褪色,但褪色的原理是不同的 | |
| C. | 用溴水可以鉴别乙烯与乙炔 | |
| D. | 苯和苯的同系物都可以用酸性高锰酸钾溶液鉴别 |
6.有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是( )
| 方案 | 操作 | 判断 |
| A | 分别加入澄清石灰水 | 产生沉淀者为Na2CO3 |
| B | 分别加入等浓度的稀盐酸 | 反应较剧烈者为Na2CO3 |
| C | 分别加入CaCl2溶液 | 产生沉淀者为Na2CO3 |
| D | 逐渐加入等浓度的盐酸 | 立即产生气泡者为Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |