题目内容
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按下列框图进行反应.又知E溶液是无色溶液.请回答:
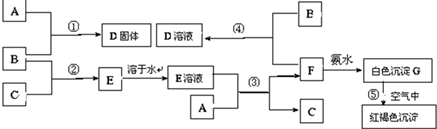
请回答:(1)(写化学式)A是 ,B是 ,C是 .
(2)反应①的化学方程式 .
(3)反应③的化学方程式 .
(4)反应④的离子方程式 .
(5)反应⑤的化学方程式 .

请回答:(1)(写化学式)A是
(2)反应①的化学方程式
(3)反应③的化学方程式
(4)反应④的离子方程式
(5)反应⑤的化学方程式
考点:无机物的推断
专题:推断题
分析:单质B为黄绿色气体,可知B为Cl2;F与氨气反应生成白色沉淀G、G在空气中变为红褐色沉淀,则红褐色沉淀为Fe(OH)3,G为Fe(OH)2,根据元素守恒可知,单质A为Fe,结合转化关系可知,单质C为H2,E为HCl,F为FeCl2,D为FeCl3,据此解答.
解答:
解:(1)单质B为黄绿色气体,可知B为Cl2;F与氨气反应生成白色沉淀G、G在空气中变为红褐色沉淀,则红褐色沉淀为Fe(OH)3,G为Fe(OH)2,根据元素守恒可知,单质A为Fe,结合转化关系可知,单质C为H2,E为HCl,F为FeCl2,D为FeCl3,
故答案为:Fe;Cl2;H2;
(2)反应①的化学方程式为:2Fe+3Cl2
2FeCl3,故答案为:2Fe+3Cl2
2FeCl3;
(3)反应③的化学方程式为:Fe+2HCl=FeCl2+H2↑,故答案为:Fe+2HCl=FeCl2+H2↑;
(4)反应④的离子方程式为:2Fe2++Cl2=2Cl-+2Fe3+,故答案为:2Fe2++Cl2=2Cl-+2Fe3+;
(5)反应⑤的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
故答案为:Fe;Cl2;H2;
(2)反应①的化学方程式为:2Fe+3Cl2
| ||
| ||
(3)反应③的化学方程式为:Fe+2HCl=FeCl2+H2↑,故答案为:Fe+2HCl=FeCl2+H2↑;
(4)反应④的离子方程式为:2Fe2++Cl2=2Cl-+2Fe3+,故答案为:2Fe2++Cl2=2Cl-+2Fe3+;
(5)反应⑤的化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
点评:本题考查无机物的推断,题目难度中等,物质的颜色是推断突破口,注意对元素化合物性质的掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列是有关生活中的醋酸的应用,其中主要利用了醋酸酸性的是( )
| A、醋酸不小心滴到大理石桌面上,桌面失去光泽 |
| B、熏醋可一定程度上防止流行性感冒 |
| C、醋可以除去水壶上的水垢 |
| D、用醋烹饪鱼,除去鱼的腥味 |
下列叙述正确的是( )
| A、P4是非极性分子,磷原子处在正方形4个角上 |
| B、H2O是极性分子,氧原子不处在2个氢原子所连成的直线的中央 |
| C、CCl4是非极性分子,碳原子处在4个氯原子所组成的正方形的中心 |
| D、CO2是极性分子,碳原子处在2个氧原子所连成的直线的中央 |
| E、CO2是极性分子,碳原子处在2个氧原子所连成的直线的中央 |
室温下,在pH=2的强酸溶液中,由水电离出的c(H+)为( )
| A、1.0×10-7mol?L-1 |
| B、1.0×10-6mol?L-1 |
| C、1.0×10-2mol?L-1 |
| D、1.0×10-12mol?L- |
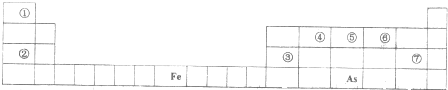
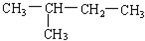 (8)
(8)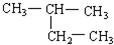 (9)新戊烷.
(9)新戊烷.