题目内容
4.下列叙述正确的是( )| A. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 没有单质参加的反应一定不是氧化还原反应 | |
| C. | 置换反应一定是氧化还原反应 | |
| D. | 化合反应一定是氧化还原反应 |
分析 氧化还原反应的特征是元素化合价的升降,氧化还原反应可发生在不同元素之间,也可以是同种元素之间,结合相关物质的性质解答该题.
解答 解:A.氯气和水发生反应时,只有氯元素化合价发生变化,故A错误;
B.存在元素化合价的变化的反应是氧化还原反应,如二氧化硫与双氧水反应生成硫酸和水,没有单质参加,属于氧化还原反应,故B错误;
C.置换反应有单质参加和生成,元素化合价一定发生变化,一定属于氧化还原反应,故C正确;
D.存在元素化合价的变化的反应是氧化还原反应,氨气与HCl化合生成氯化铵,是化合反应,不是氧化还原反应,故D错误.
故选C.
点评 本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,注意从元素化合价的角度认识氧化还原反应相关概念,答题时注意能举出实例,难度不大.

练习册系列答案
相关题目
15.有关下如图所示原电池的叙述不正确的是( )
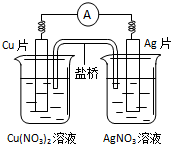

| A. | 电子沿导线由Cu片流向Ag片 | |
| B. | 正极的电极反应是Ag++e-=Ag | |
| C. | Cu片上发生氧化反应,Ag片上发生还原反应 | |
| D. | 反应时盐桥中的阳离子移向Cu(NO3)2溶液 |
12.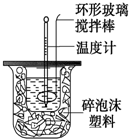 测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )
测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )
 测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )
测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )| A. | 实验中使用的搅拌棒材料为铁 | |
| B. | 读取温度计读数时,读取的是混合溶液的最高温度 | |
| C. | 分多次把NaOH溶液倒入盛有硫酸的小烧杯中 | |
| D. | 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
19.世界卫生组织对塑化剂DEHP(分子式为C24H38O4)规定的每日耐受摄入量为每千克0.025毫克,以体重为78kg的成人来讲,每天摄入1.95毫克及以下的DEHP是安全的.体重为78kg的成人每天摄入下列DEHP时,不安全的是(设NA为阿伏加德罗常数的值)( )
| A. | 5×10-6NA个DEHP分子 | |
| B. | 含有1.2×10-4NA个碳原子的DEHP分子 | |
| C. | 含有2×10-5NA个氧原子的DEHP分子 | |
| D. | 含有2.0×10-4NA个氢原子的DEHP分子 |
16.下列分离物质的方法中,根据微粒大小进行分离的是( )
| A. | 萃取 | B. | 蒸馏 | C. | 分液 | D. | 渗析 |
13.、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系.若25℃时有HA?H++A-,则K=$\frac{c({H}^{+})•c({A}^{-})}{c(HA)}$.式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度.下表是几种常见弱酸的电离平衡常数(25℃).
回答下列问题:
(1)当升高温度时,K值变大(填“变大”“变小”或“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?K值越大电离出的氢离子浓度越大,所以酸性越强.
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看做是酸,其中酸性最强的是H3PO4,最弱的是HPO42-.
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是K1:K2:K3≈1:10-5:10-10,产生此规律的原因是上一级电离产生的H+对下一级电离有抑制作用.
(5)Na2CO3溶液呈碱性(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是CO32-+H2O?HCO3-+OH-.
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)小于c(HPO42-)(填“大于”或“小于”).
| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COOH-+H+ | 1.76×10-5 |
| H2CO3 | H2CO3?H++HCO3-HCO3-?H++HCO32- | K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?H++HS-HS-?H++S2- | K1=9.1×10-8 K2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4-H2PO4-H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3K2=6.23×10-8 K3=2.20×10-13 |
(1)当升高温度时,K值变大(填“变大”“变小”或“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?K值越大电离出的氢离子浓度越大,所以酸性越强.
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看做是酸,其中酸性最强的是H3PO4,最弱的是HPO42-.
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是K1:K2:K3≈1:10-5:10-10,产生此规律的原因是上一级电离产生的H+对下一级电离有抑制作用.
(5)Na2CO3溶液呈碱性(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是CO32-+H2O?HCO3-+OH-.
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)小于c(HPO42-)(填“大于”或“小于”).
