题目内容
18.在298K、100kPa时,已知:H2O(g)=$\frac{1}{2}$O2(g)+H2(g)△H1H2(g)+Cl2(g)═2HCl(g)△H2
2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
| A. | △H3=2△H1+2△H2 | B. | △H3=2△H1-△H2 | C. | △H3=2△H1-2△H2 | D. | △H3=2△H1+△H2 |
分析 ①H2O(g)=$\frac{1}{2}$O2(g)+H2(g)△H1;
②H2(g)+Cl2(g)═2HCl(g)△H2;
③2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3;
依据盖斯定律①×2+②×2得到:2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)据此计算.
解答 解:由①H2O(g)=$\frac{1}{2}$O2(g)+H2(g)△H1;
②H2(g)+Cl2(g)═2HCl(g)△H2;
③2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3;
依据盖斯定律①×2+②×2得到:2H2O(g)+2Cl2(g)═4HCl(g)+O2(g),即△H3=2△H1+2△H2.
故选A.
点评 本题考查了盖斯定律的应用,题目难度不大,明确盖斯定律的含义即可解答,注意教材知识的灵活应用是解题关键,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
8.同分异构体具有相同的:①最简式 ②分子式 ③相对分子质量 ④化学性质 ⑤物理性质( )
| A. | ①②③ | B. | ②⑤ | C. | ②④⑤ | D. | ②③④ |
9.X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
(1)Q在元素周期表中的位置是第二周期VIA族.
(2)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,则M的氧化物与强碱溶液反应的离子方程式是BeO+2OH-=BeO22-+H2O.
(3)Q和R按原个数比1:1组成的化合物甲是一种“绿色”氧化剂.甲中所含共价键类型是极性键、非极性键.
(4)Z与Q的最简单氢化物中沸点较高的是H2O(填化学式),原因是H2O分子之间存在氢键作用.
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(2)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,则M的氧化物与强碱溶液反应的离子方程式是BeO+2OH-=BeO22-+H2O.
(3)Q和R按原个数比1:1组成的化合物甲是一种“绿色”氧化剂.甲中所含共价键类型是极性键、非极性键.
(4)Z与Q的最简单氢化物中沸点较高的是H2O(填化学式),原因是H2O分子之间存在氢键作用.
6.下列表示的是化学反应 A+2B═C+D 在不同条件下的反应速率,其中最快的是( )
| A. | v(A)=0.3mol?L-1?s-1 | B. | v(B)=0.5mol?L-1?s-1 | ||
| C. | v(C)=0.25mol?L-1?s-1 | D. | v(D)=0.2mol?L-1?s-1 |
13.下列描述中正确的是( )
| A. | ClO3-的空间构型为平面三角形 | |
| B. | 乙炔分子中的两个碳原子采用sp2杂化方式 | |
| C. | CS2为V形的极性分子 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
3.下列实验中,操作和现象均正确且能实现相应实验目的是( )
| 选项 | 实验目的 | 操作 | 现象 |
| A | 验证BaSO3难溶于水 | 将SO2通入Ba(NO3)2溶液中 | 有白色沉淀生成 |
| B | 验证非金属性:Br>I | 将溴水滴加到淀粉KI溶液中 | 溶液变蓝 |
| C | 验证SO2的漂白性 | 将SO2通入氯水中 | 氯水褪色 |
| D | 验证某化合物是钠盐 | 将该化合物在酒精灯上灼烧 | 焰色为黄色 |
| A. | A | B. | B | C. | C | D. | D |
10.短周期元素X和Y,可组成化合物XY3.当X的原子序数为a时,Y的原子序数可能是:①a+2,②a+4,③a+8,④a+12,⑤a-6,其中正确的组合是( )
| A. | ①② | B. | ①②③ | C. | ①②③⑤ | D. | ①②④⑤ |
7.下列说法不正确的是( )
| A. | 通过对苯燃烧和甲烷燃烧现象的对比,可以判断两种物质中含碳量的高低 | |
| B. | 苯不能使酸性高锰酸钾溶液褪色,说明苯分子中没有碳碳双键 | |
| C. | 甲烷分子是空间正四面体形,苯分子是平面形 | |
| D. | 苯不能与Br2(CCl4)发生加成反应,故苯为饱和烃 |
13.已知还原性:SO32->I-.某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如图实验:下列说法正确的是( )
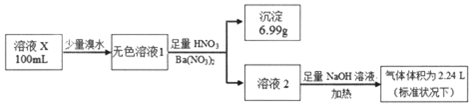

| A. | 溶液X肯定只存在NH4+、SO42- | |
| B. | 溶液X一定不含有Ba2+、Fe3+,可能含有I- | |
| C. | 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液 | |
| D. | 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧 |