题目内容
9.X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
(2)周期表中有些处于对角(左上→右下)位置的元素,它们的单质及其化合物的性质存在“对角线相似”的现象,则M的氧化物与强碱溶液反应的离子方程式是BeO+2OH-=BeO22-+H2O.
(3)Q和R按原个数比1:1组成的化合物甲是一种“绿色”氧化剂.甲中所含共价键类型是极性键、非极性键.
(4)Z与Q的最简单氢化物中沸点较高的是H2O(填化学式),原因是H2O分子之间存在氢键作用.
分析 X和M的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知M为Be,X为Mg,Q和Z的化合价都有-2价,应为周期表第ⅥA族元素,Z的最高价为+6价,应为S元素,Q无正价,应为O元素,Y的化合价为+3价,应为周期表第ⅢA族元素,根据半径X大于Y可知应和X同周期,为Al元素,R的原子半径最小,元素的化合价为+1价,R为H,结合元素周期律知识解答该题.
解答 解:由上述分析可知,X为Mg,Y为Al,Z为S,M为Be,Q为O,R为H,
(1)Q在元素周期表中的位置是第二周期VIA族,故答案为:第二周期VIA族;
(2)M的氧化物与强碱溶液反应的离子方程式是BeO+2OH-=BeO22-+H2O,故答案为:BeO+2OH-=BeO22-+H2O;
(3)Q和R按原个数比1:1组成的化合物甲是一种“绿色”氧化剂,甲为H2O2,所含共价键类型是极性键、非极性键,故答案为:极性键、非极性键;
(4)Z与Q的最简单氢化物中沸点较高的是H2O,因H2O分子之间存在氢键作用,故答案为:H2O;H2O分子之间存在氢键作用.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意对角线规则的应用,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
19. 为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
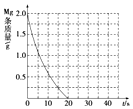
②若①中实验a镁条消失的时间是20s,则镁条剩余质量与时间关系图如图.
假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的$\frac{1}{2}$,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注.
 为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,准备了以下化学用品:0.20mol•L-1与0.40mol•L-1的HCl溶液、0.20mol•L-1与0,.40mol•L-1的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.①酸液都取足量、相同体积,请你帮助完成以下实验设计表:
| 实验 编号 | 温度(K) | 盐酸浓度/ (mol•L-1) | 醋酸浓度/ (mol•L-1) | 实验目的 |
| a | 298 | 0.20 | I.实验a和b是探究温度 对镁与盐酸反应速率的影响; II.实验a和c是探究浓度 对镁与盐酸反应速率的影响; III.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别 | |
| b | 308 | 0.20 | ||
| c | 298 | 0.40 | ||
| d | -- | -- |
假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同时,醋酸是相同浓度盐酸平均速度的$\frac{1}{2}$,请在此图中大致画出“实验b”、“实验d”的镁条剩余质量与时间关系曲线,请注意必要的标注.
20.绿色化学提倡化工生产应提高原子利用率.原子利用率表示目标产物的质量与生成物总质量之比.在下列氮肥的制备反应中,原子利用率最高的是( )
| A. | NH3+H2O+CO2=NH4HCO3 | |
| B. | 2NH3+CO2$\frac{\underline{\;180-200℃\;}}{15-30MPa}$ CO(NH2)2+H2O | |
| C. | 8NH3+3Cl2═N2+6NH4Cl | |
| D. | 2NH3+2O2$\frac{\underline{\;一定条件\;}}{\;}$NH4NO3+H2O |
17.A、B两种有机物组成的混合物,当混合物总质量一定时,无论A、B以何种比例混合,完全燃烧后,生成CO2的质量为定值,则符合这一条件的有机物组合是( )
| A. | 甲醇(CH3OH)和乙二醇(HOCH2CH2OH) | B. | 甲醛(HCHO)和乙醛 (CH3CHO) | ||
| C. | CH4和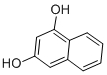 | D. | 苯(C6H6)和苯酚(C6H5OH) |
4.根据下列实验操作和现象,所得结论正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 该溶液中含有SO${\;}_{4}^{2-}$、SO${\;}_{3}^{2-}$、HSO${\;}_{3}^{-}$中的一种或几种 |
| B | 将蘸有浓氨水的玻璃棒靠近蘸有某溶液的玻璃棒 | 有白烟产生 | 该溶液是浓盐酸 |
| C | 将某气体通入品红溶液中 | 溶液红色褪去 | 该气体可能是SO2 |
| D | 向某溶液中滴加稀NaOH溶液时,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 该溶液中不含NH${\;}_{4}^{+}$ |
| A. | A | B. | B | C. | C | D. | D |
14.下列分子中,空间构型为v型的是( )
| A. | NH3 | B. | CCl4 | C. | H2O | D. | CH2O |
1.下列物质中,属于共价化合物的是( )
| A. | 氯化镁 | B. | 二氧化碳 | C. | 氢气 | D. | 硫酸铜 |
18.在298K、100kPa时,已知:H2O(g)=$\frac{1}{2}$O2(g)+H2(g)△H1
H2(g)+Cl2(g)═2HCl(g)△H2
2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
H2(g)+Cl2(g)═2HCl(g)△H2
2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
| A. | △H3=2△H1+2△H2 | B. | △H3=2△H1-△H2 | C. | △H3=2△H1-2△H2 | D. | △H3=2△H1+△H2 |
4.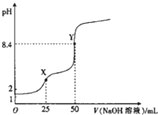 用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )
用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )
 用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )
用0.1mot•L-1的NaOH溶液滴定25mL0.1mol•L-1 H2C2O4(草酸)溶液的滴定曲线如图所示,下列说法不正确的是( )| A. | 草酸是弱酸 | |
| B. | X点:c(H2C2O4)+c(HC2O4-)=c (Na+)-c(C2O42-) | |
| C. | Y 点:c(H2C2O4)+c(HC2O4-)=c(OH-)-C(H+) | |
| D. | 滴定过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+) |