题目内容
下列有关实验装置的说法,不正确的是( )
A、 装置制取收集干燥纯净的NH3 |
B、 装置可进行碘水中碘的萃取及分液 |
C、 检查此装置的气密性 |
D、 称NaOH固体的质量 |
考点:化学实验方案的评价
专题:
分析:A.浓氨水与NaOH可制取氨气,氨气利用碱石灰干燥,最后利用向下排空气法收集;
B.图中为萃取、分液装置;
C.加水,利用液柱的高度在一段时间不变检验气密性;
D.称量时左物右码,且NaOH应在烧杯中称量.
B.图中为萃取、分液装置;
C.加水,利用液柱的高度在一段时间不变检验气密性;
D.称量时左物右码,且NaOH应在烧杯中称量.
解答:
解:A.浓氨水与NaOH可制取氨气,氨气利用碱石灰干燥,最后利用向下排空气法收集,图中制备及收集合理,故A正确;
B.碘不易溶于水,易溶于有机溶剂,则图中为萃取、分液装置可分离,故B正确;
C.加水,利用图中右侧中液面的高度差在一段时间不变检验气密性,故C正确;
D.称量时左物右码,且NaOH应在烧杯中称量,则NaOH应在左侧烧杯中称量,故D错误;
故选D.
B.碘不易溶于水,易溶于有机溶剂,则图中为萃取、分液装置可分离,故B正确;
C.加水,利用图中右侧中液面的高度差在一段时间不变检验气密性,故C正确;
D.称量时左物右码,且NaOH应在烧杯中称量,则NaOH应在左侧烧杯中称量,故D错误;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及实验基本操作和实验基本技能等,把握实验基本操作和图中装置的作用为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
下列实验操作中错误的是( )
| A、萃取操作时,所选萃取剂必须与原溶剂互不相溶 |
| B、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| D、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
乙硼烷常温下一种毒性很大的易燃气体,在近代工业和军事上具有重要用途,主要用于火箭和导弹的高能燃料.0.3mol的高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固体B2O3和液态水,放出649.5KJ的热量.下列关于乙硼烷的叙述正确的是.
| A、B2H6固体时为原子晶体 |
| B、乙硼烷在军事上具有重要用途是因为它有剧毒. |
| C、乙硼烷的燃烧热为2165KJ/mol |
| D、乙硼烷燃烧的热化学方程式为B2H6(g)+3O2(g)═B2O3(S)+3H2O(g)△H=0.165KJ/mol |
已知298K时,Zn(s)+0.5O2(g)═ZnO(s)△H1=-351.1kJ?mol-1,
Hg(l)+0.5O2(g)═HgO(s)△H2=-90.7kJ?mol-1.
求Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H的值为( )
Hg(l)+0.5O2(g)═HgO(s)△H2=-90.7kJ?mol-1.
求Zn(s)+HgO(s)═ZnO(s)+Hg(l)△H的值为( )
| A、-441.8 kJ?mol-1 |
| B、260.4 kJ?mol-1 |
| C、-254.6 kJ?mol-1 |
| D、-260.4 kJ?mol-1 |
 如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种试验某气体化学性质的实验装置,图中B为开关. 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )| A、浓H2SO4 |
| B、饱和Na2CO3溶液 |
| C、浓NaOH溶液 |
| D、饱和NaCl溶液 |
25℃时,20mL硫酸和硝酸的混合溶液,加入足量的氯化钡溶液,充分反应后过滤、洗涤、烘干,可得0.466g沉淀.滤液跟2mol/L NaOH溶液反应,用去10.00mL碱液时恰好中和.下列说法中正确的是( )
| A、原混合液中c(SO42-)=0.2 mol/L |
| B、原混合液中c(NO3-)=0.9 mol/L |
| C、原混合液中pH=0 |
| D、原混合液中由水电离出的c(H+)=0.1 mol/L |
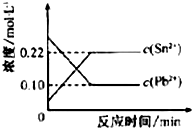 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A、往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B、往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C、升高温度,平衡体系中c(Pb2+)增大,说明该反应为吸热反应 |
| D、25℃时,该反应的平衡常数K=2.2 |

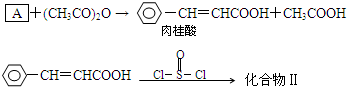
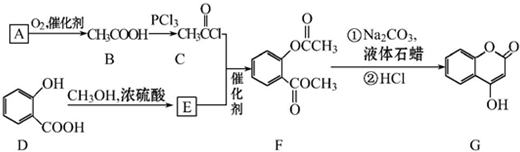
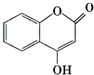 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: