��Ŀ����
13���Ի�ͭ����Ҫ�ɷ���FeCuS2����ͭ��ԼΪ1%��Ϊԭ���Ʊ�ͭ��ұ��ͭ��-�ַ������������������£�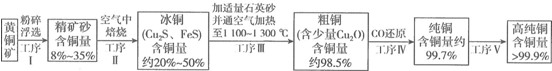
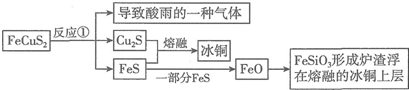
��1��������漰����Ҫ��Ӧ�������£�
��Ӧ�ٲ����ġ����������һ�����塱�γɵ����꣬ij����С��ⶨ���������pH���֣�����ʱ�������pH��С���û�ѧ����ʽ��ʾ
pH��С��ԭ��2H2SO3+O2=2H2SO4��
��2������III�漰����Ҫ��Ӧ�������У�
�١�Cu2S+��O2$\frac{\underline{\;\;��\;\;}}{\;}$��Cu2O+��SO2���뽫��ƽ��Ļ�ѧ���������뷽���У��õ����ű������ת�Ƶķ������Ŀ��
���ڷ�ӦCu2O+Cu2S$\frac{\underline{\;\;��\;\;}}{\;}$Cu+SO2����δ��ƽ���У�������1molSO2������6 mol+l�۵�ͭ����ԭ��
��ʯӢɰ����Ҫ�ɷ���SiO2��1mol����Ҫ�ɷ��к��еĻ�ѧ��Ϊ4 NA����ʾ����٤������������������ʯӢɰ��Ŀ������FeO�γ�¯��FeSiO3��������ȥ����FeS
��3������V���������������ǵ�⾫����
��4��ұ�������еķ������պ��������Ʊ����ᣮ
���� ��1�����������γɵ�����ɷ��к��������ᣬ��������һ�����ᣬ�ڿ������ܱ�����Ϊǿ�����ᣬ��Һ��������ǿ��pH��С��
��2�������ù۲취��ƽ����Ӧ��������Ԫ��ʧȥ���ӣ���Ԫ�صõ����ӣ�
�����ù۲취��ƽ��2Cu2O+Cu2S$\frac{\underline{\;\;��\;\;}}{\;}$6Cu+SO2����������1molSO2������ 6mol+l�۵�ͭ����ԭ��
��1mol���������к���4mol�������������������FeO��Ӧ��FeO+SiO2$\frac{\underline{\;����\;}}{\;}$FeSiO3����Ϊ¯����������ȥ����FeS��
��3���ɴ�ͭ�Ƹߴ�ͭ���õ�⾫����
��4����������Ҫ�ɷ��Ƕ����������ڹ�ҵ�����ᣮ
��� �⣺��1����ҵ�����в����˶��������������γɵ�����ɷ��к��������ᣬ��������һ�����ᣬ�ڿ������ܱ�����Ϊǿ�����ᣬ��Һ��������ǿ��pH��С��
�ʴ�Ϊ��2H2SO3+O2=2H2SO4��
��2�������ù۲취��ƽ����Ӧ��������Ԫ��ʧȥ���ӣ���Ԫ�صõ����ӣ�����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
�����ù۲취��ƽ��2Cu2O+Cu2S$\frac{\underline{\;\;��\;\;}}{\;}$6Cu+SO2����������1molSO2������ 6mol+l�۵�ͭ����ԭ��
�ʴ�Ϊ��6��
��1mol���������к���4mol�������������������FeO��Ӧ��FeO+SiO2$\frac{\underline{\;����\;}}{\;}$FeSiO3����Ϊ¯����������ȥ����FeS��
�ʴ�Ϊ����FeO�γ�¯��FeSiO3��������ȥ����FeS��
��3���ɴ�ͭ�Ƹߴ�ͭ���õ�⾫����
�ʴ�Ϊ����⾫����
��4����������Ҫ�ɷ��Ƕ����������ڹ�ҵ�����
�ʴ�Ϊ�����ᣮ
���� ���⿼����Ԫ�ػ���������ʣ��ۺϿ�������֪ʶǨ�Ʒ�������������������ѧ�������������нϸߵ�Ҫ��

| A�� | �ֻ����� | B�� | ����ֽ | C�� | �л����� | D�� | ˮ���� |
| A�� | KCl | B�� | CuSO4 | C�� | AgNO3 | D�� | H2SO4 |
�����÷�Һ������ʴҺ
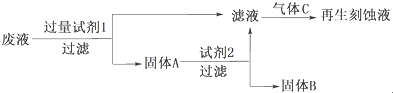
��1���Լ�2��HCl������B��Cu��ͨ�������C��Cl2�����ѧʽ��
��2��д�������Լ�1������Ӧ�����ӷ���ʽ��Fe+2Fe3+=3Fe2+��Fe+Cu2+=Fe2++Cu��
�����÷�Һ�Ʊ�CuCl2•2H2O����
��֪���йؽ������Ӵӿ�ʼ������������ȫʱ��Һ��pH��
| Fe3+ | Cu2+ | Fe2+ | |
| ��ʼ������pH | 2.7 | 5.4 | 8.1 |
| ������ȫ��pH | 3.7 | 6.9 | 9.6 |

��1��Ϊȷ����Ʒ�Ĵ��ȣ��Լ�1ΪB���Լ�2ΪD������ĸ����
A��KMnO4 B��H2O2 C��NaOH D��Cu2��OH��2CO3
��2������A�Ļ�ѧʽΪFe��OH��3��ΪʹA��ȫ����������pH�ķ�Χ��[3.7��5.4����
��3������������Ϊ����Ũ������ȴ�ᾧ�����ˣ������������������õ��Ĺ�������������©�����ձ����ƾ����⣬����Ҫ������������
��4��ʹ����ˮ�Ҵ�����ˮ����ϴ�ӵ��ŵ��Ǽ���CuCl2•2H2O ������ˮ����ʧ���������ں������
| A�� | ������Ԫ����ǽ���Ԫ��֮�䶼�γ����Ӽ� | |
| B�� | �γ����Ӽ����������ǽ����������������� | |
| C�� | �������Ӽ��Ļ������У�Ҳ���ܻ����й��ۼ� | |
| D�� | �ǽ���Ԫ���γɵĻ�����һ�����������Ӽ� |
| A�� | NH4H�ǹ��ۻ����� | B�� | NH4H����ˮ�����γɵ���Һ�Լ��� | ||
| C�� | NH4H��ˮ��Ӧʱ��ˮ����ԭ�� | D�� | NH4H�е�HԪ��ֻ��һ�ֻ��ϼ� |