题目内容
NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、16克氧气所含的氧原子数为2NA |
| B、18克水所含的电子数为NA |
| C、2.4克金属钠与足量盐酸反应失去的电子数为0.1NA |
| D、17克氢氧根离子所含的电子数为10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.16g氧气中含有16g氧原子,含有1mol氧原子;
B.水分子中含有10个电子,18g水的物质的量为1mol,含有10mol电子;
C.钠为1价金属,2.4g钠的物质的量大于0.1mol,完全反应失去电子的物质的量大于0.1mol;
D.氢氧根离子中含有10个电子,17g氢氧根离子的物质的量为1mol,含有10mol电子.
B.水分子中含有10个电子,18g水的物质的量为1mol,含有10mol电子;
C.钠为1价金属,2.4g钠的物质的量大于0.1mol,完全反应失去电子的物质的量大于0.1mol;
D.氢氧根离子中含有10个电子,17g氢氧根离子的物质的量为1mol,含有10mol电子.
解答:
解:A.16g氧气含有16gO,含有氧原子的物质的量为1mol,所含的氧原子数为NA,故A错误;
B.18g水的物质的量为1mol,1mol水中含有10mol电子,所含的电子数为10NA,故B错误;
C.2.4g钠的物质的量大于0.1mol,所以2.4g钠完全反应失去的电子的物质的量大于0.1mol,失去的电子数大于0.1NA,故C错误;
D.17g氢氧根离子的物质的量为1mol,1mol氢氧根离子中含有10mol电子,所含的电子数为10NA,故D正确;
故选D.
B.18g水的物质的量为1mol,1mol水中含有10mol电子,所含的电子数为10NA,故B错误;
C.2.4g钠的物质的量大于0.1mol,所以2.4g钠完全反应失去的电子的物质的量大于0.1mol,失去的电子数大于0.1NA,故C错误;
D.17g氢氧根离子的物质的量为1mol,1mol氢氧根离子中含有10mol电子,所含的电子数为10NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项C为易错点,注意钠的质量与摩尔质量的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
Fe、Mg、Al三种金属分别与1mol/L的盐酸反应,产生的氢气体积相同(相同状况),则参加反应的金属( )
| A、质量相等 |
| B、物质的量相等 |
| C、失电子数相等 |
| D、反应速度相等 |
下列属于电离方程式且书写正确的是( )
| A、2H2O=2H2↑+O2↑ |
| B、Ba(OH)2=Ba2++OH- |
| C、H2SO4=2H++SO42- |
| D、NaHCO3=Na++H++CO32- |
等体积的硫酸钠、硫酸镁、硫酸铝溶液分别于足量氯化钡溶液反应,若生成硫酸钡的质量相等,则三种硫酸盐的物质的量浓度之比为( )
| A、3:3:1 |
| B、6:3:2 |
| C、3:2:1 |
| D、1:1:1 |
常温时,下列关于电解质溶液的叙述正确的是( )
| A、稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B、常温下物质的量浓度相等的①(NH4)2CO3、②NH4A1(SO4)2、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):③>①>② |
| C、pH=ll的NaOH和pH=ll的氨水分别稀释100倍后的pH前者一定大于后者 |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
下列实验操作中,错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出后,换个洁净的烧杯,将上层液体从上口放入烧杯中 |
| B、蒸馏时,应使温度计水银球位于蒸馏烧瓶支管口处 |
| C、用酒精萃取溴水溶液中的溴 |
| D、称量时,将称量物体放在称量纸或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
常温下,某无色溶液中由水电离产生的c(H+)=10-12mol/L,则此溶液中一定能大量共存的离子组是( )
| A、Mg2+、NH4+、K+、SO42- |
| B、Na+、S2O32-、OH-、Br- |
| C、Na+、K+、NO3-、SO42- |
| D、K+、Cr2O72-、NO3-、Cl- |
下列实验装置或操作能达到实验目的是( )
A、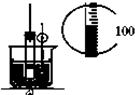 实验室制硝基苯 |
B、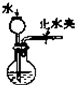 检查装置气密性 |
C、 利用排空气法收集丙烷 |
D、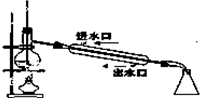 石油分馏 |
“钴酞菁(分子直径1.3×10-9m)”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似,我国科学家在世界上第一次为“钴酞菁”分子恢复了磁性.下列关于“钴酞菁”的说法正确的是( )
| A、在水中形成的分散系属于悬浊液 |
| B、分子直径比Na+小 |
| C、“钴酞菁”分子不能透过滤纸 |
| D、在水中形成的分散系具有丁达尔效应 |