题目内容
下列溶液中,溶质的物质的量浓度为1mol?L-1 的是( )
| A、将40 g NaOH溶于1 L 水所得的溶液 |
| B、将0.5 mol?L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液 |
| C、将31 g Na2O 溶于水并配成1 L的溶液 |
| D、含K+为1mol?L-1的K2SO4溶液 |
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:A.溶液的体积不等于溶剂的体积;
B.蒸发前后溶液密度不同,体积不等于50mL;
C.根据质量计算生成NaOH的物质的量,进而计算浓度;
D.根据c(K2SO4)=
c(K+)计算.
B.蒸发前后溶液密度不同,体积不等于50mL;
C.根据质量计算生成NaOH的物质的量,进而计算浓度;
D.根据c(K2SO4)=
| 1 |
| 2 |
解答:
解:A.溶液的体积不等于溶剂的体积,所得溶液的浓度不等于1mol/L,故A错误;
B.蒸发前后溶液密度不同,体积不等于50mL,故B错误;
C.31 g Na2O 的物质的量为0.5mol,与水反应生成NaOH 1mol,配成1L溶液,浓度为1mol/L,故C正确;
D.c(K2SO4)=
c(K+)=0.5mol/L,故D错误.
故选C.
B.蒸发前后溶液密度不同,体积不等于50mL,故B错误;
C.31 g Na2O 的物质的量为0.5mol,与水反应生成NaOH 1mol,配成1L溶液,浓度为1mol/L,故C正确;
D.c(K2SO4)=
| 1 |
| 2 |
故选C.
点评:本题考查学生对物质的量浓度的理解,难度不大,注意A选项为易错点,注意溶液的体积与溶剂体积的区别,注意对物质的量浓度定义式的理解.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
下列说法正确的是( )
| A、在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| B、C2H6O和C4H10都有2种同分异构体 |
| C、乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D、淀粉和蛋白质均可水解生成葡萄糖 |
下列现象或应用中,不能用胶体知识解释的是( )
| A、在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
| B、用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
| C、清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱 |
| D、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
下列溶液中,跟100mL 0.5mol?L-1NaCl溶液所含的Cl-物质的量浓度相同的是( )
| A、100mL 0.5mol?L-1MgCl2溶液 |
| B、200mL 0.25mol?L-1CaCl2溶液 |
| C、50mL 1mol?L-1NaCl溶液 |
| D、25mL 0.5mol?L-1HCl溶液 |
下列四种模型仅由C、H、O三种原子组成,下列说法正确的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  | 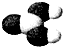 |
| A、模型1对应的物质含有双键 |
| B、1mol模型2对应的物质与足量的银氨溶液充分反应,能生成216gAg |
| C、模型3对应的物质在一定条件下能发生银镜反应 |
| D、模型3、模型4对应的物质均具有酸性,且酸性4强于3 |
下列过程中,涉及化学变化的是( )
| A、三氯化铁溶液滴入沸水中制胶体 |
| B、氯化钠溶于水 |
| C、过滤除去粗盐中的不溶性杂质 |
| D、蒸馏法将海水淡化为饮用水 |
 新型纳米材料氧缺位铁酸盐(MFe2OX)(3<x<4;M表示Mn、Co、Zn或Ni的二价离子),常温下,它使能工业废气中的SO2、NO2等氧化物转化为单质.转化流程如图所示:
新型纳米材料氧缺位铁酸盐(MFe2OX)(3<x<4;M表示Mn、Co、Zn或Ni的二价离子),常温下,它使能工业废气中的SO2、NO2等氧化物转化为单质.转化流程如图所示: