题目内容
下表是某矿物质饮用水的部分标签说明,则该饮用水中还可能较大量存在的离子是( )
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
| A、Ca2+ |
| B、Na+ |
| C、OH- |
| D、Ag+ |
考点:离子共存问题
专题:
分析:根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:A.Ca2+与SO42-结合生成沉淀,不能共存,故A错误;
B.钠离子与水中离子均不反应,可大量共存,故B正确;
C.Mg2+与OH-结合生成沉淀,不能共存,故C错误;
D.Cl-与Ag+结合生成沉淀,不能共存,故D错误;
故选B.
B.钠离子与水中离子均不反应,可大量共存,故B正确;
C.Mg2+与OH-结合生成沉淀,不能共存,故C错误;
D.Cl-与Ag+结合生成沉淀,不能共存,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
香叶醇是合成玫瑰香油的主要原料,其结构简式如图: 下列有关香叶醇的叙述错误的是( )
下列有关香叶醇的叙述错误的是( )
 下列有关香叶醇的叙述错误的是( )
下列有关香叶醇的叙述错误的是( )| A、香叶醇的分子式为C10H19O |
| B、能使溴的四氯化碳溶液褪色 |
| C、能使酸性高锰酸钾溶液褪色 |
| D、能发生取代反应,也能发生1,4加成反应 |
关于图中各装置的叙述不正确的是( )


| A、装置①是中和滴定法测定硫酸的物质的量浓度 |
| B、装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气 |
| C、装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| D、装置④证明铁生锈过程中空气参与反应 |
设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、在0.1mol氢氧化钠中,阴、阳离子的个数比为1:1 |
| B、标准状况下,如果11.2LO2含有n个氧分子,则NA为2n |
| C、22.4L氢气所含原子数目为2NA |
| D、标准状况下,18克的水物质的量为1mol |
实验室里由粗盐制备精盐的实验中,必需的操作步骤有( )
| A、溶解 | B、过滤 |
| C、分液 | D、蒸发浓缩 |
下列叙述正确的是( )
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、乙烯和乙烷都能发生加聚反应 |
| D、石油的裂解是物理变化 |
如图为雾霾的主要成分示意图.下列说法不正确的是( )
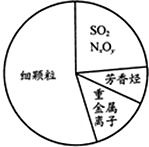

| A、重金属离子可导致蛋白质变性 |
| B、苯是最简单的芳香烃 |
| C、SO2和NxOy都属于酸性氧化物 |
| D、汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
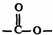 基团:
基团: