题目内容
实验室里由粗盐制备精盐的实验中,必需的操作步骤有( )
| A、溶解 | B、过滤 |
| C、分液 | D、蒸发浓缩 |
考点:粗盐提纯
专题:
分析:实验室里由粗盐制备精盐的实验中,首先将粗盐溶解,然后加入除杂试剂将杂质离子变成沉淀,然后通过过滤除去难溶物,最后对滤液进行蒸发浓缩达到纯净的氯化钠,据此进行解答.
解答:
解:粗盐提纯过程为:溶解粗盐,加入试剂将杂质离子除去,接着过滤除去难溶物、泥沙等,加入盐酸调节溶液pH,除去过量的除杂试剂,最后通过蒸发浓缩达到纯净的氯化钠,所以必需的操作为:溶解、过滤、蒸发浓缩,
故选ABD.
故选ABD.
点评:本题考查了粗盐的提纯方法,题目难度不大,注意掌握粗盐提纯过程中除杂试剂的选用及除杂试剂的加入顺序,明确除杂原则.

练习册系列答案
相关题目
某有机物其结构简式如图,关于该有机物下列叙述正确的是( )
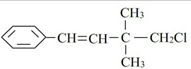

| A、不能使酸性KMnO4溶液褪色 |
| B、不能发生取代反应 |
| C、在加热和催化剂作用下,最多能和4 mol H2反应 |
| D、一定条件下,能和NaOH醇溶液反应 |
如图所示对实验Ⅰ~Ⅳ的实验现象预测正确的是( )
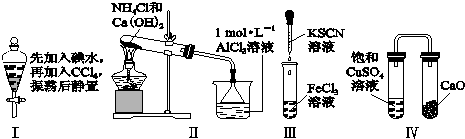

| A、实验Ⅰ:液体分层,下层呈无色 |
| B、实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C、实验Ⅲ:试管中立刻出现红色沉淀 |
| D、实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
下表是某矿物质饮用水的部分标签说明,则该饮用水中还可能较大量存在的离子是( )
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
| A、Ca2+ |
| B、Na+ |
| C、OH- |
| D、Ag+ |
下列方程式不能正确解释相关事实的是( )
A、碳酸的酸性强于苯酚:CO2+H2O+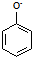 → →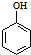 +HCO3- +HCO3- | ||||
B、工业上用氧化铝冶炼金属铝:2Al2O3(熔融)
| ||||
C、浓硫酸具有强氧化性:C+2H2SO4(浓)
| ||||
| D、金属铜能溶解于稀硝酸:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
化学与生产、生活、社会密切相关.下列有关说法错误的是( )
| A、松花蛋是一种常用食品,食用时有氨的气味,可以蘸些食醋除去 |
| B、“皮革奶”是奶粉中掺入皮革下脚料,将皮革灼烧时有烧焦羽毛的气味 |
| C、腌制食品中应严格控制NaNO2的用量 |
| D、从海水中可提取Mg,用惰性电极电解熔融的MgCl2或其水溶液都可制得Mg |
化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A、棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 |
| B、石油干馏可得到石油气、汽油、煤油、柴油等 |
| C、从海水中提取物质都必须通过化学反应才能实现 |
| D、纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |
下列变化只需通过一步化合反应就可以实现的是( )
| A、FeCl3→FeCl2 |
| B、Al2O3→Al(OH)3 |
| C、SiO2→H2SiO3 |
| D、S→SO3 |
在相同温度下用惰性电极电解下列物质的水溶液,一段时间后溶液酸性增强或碱性减弱的是( )
| A、HCl |
| B、NaOH |
| C、Na2SO4 |
| D、CuSO4 |