题目内容
关于图中各装置的叙述不正确的是( )


| A、装置①是中和滴定法测定硫酸的物质的量浓度 |
| B、装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气 |
| C、装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| D、装置④证明铁生锈过程中空气参与反应 |
考点:化学实验方案的评价
专题:
分析:A.根据氢氧化钠应盛放在碱式滴定管中,不能放在酸式滴定管中;
B.装置气密性检验有多种方法,原理都是根据装置内外的压强差形成水柱或气泡;
C.根据装置②可以吸收易溶于水的气体,并可防倒吸;
D.铁生锈过程中,如果空气参加反应,则瓶内气体压强减小,根据瓶内气体压强和大气压强的关系判断U型管内液体的变化.
B.装置气密性检验有多种方法,原理都是根据装置内外的压强差形成水柱或气泡;
C.根据装置②可以吸收易溶于水的气体,并可防倒吸;
D.铁生锈过程中,如果空气参加反应,则瓶内气体压强减小,根据瓶内气体压强和大气压强的关系判断U型管内液体的变化.
解答:
解:A.装置①中氢氧化钠不能放在酸式滴定管中,所以发生装置①不适合,故A错误;
B.装置②手捂烧瓶(橡胶管已被弹簧夹夹紧),烧瓶内气体受热膨胀,使集气瓶中气体压强增大,在玻璃管中形成一段水柱,说明装置气密性良好,不漏气,故B正确;
C.装置②X若为CCl4,NH3或HCl极易溶于水且不溶于CCl4的气体,可以用装置③并可防倒吸,故C正确;
D.铁生锈过程中,如果空气参加反应,则瓶内气体压强减小,小于大气压,则导致U型管内液面“左高右低”,故D正确;
故选A.
B.装置②手捂烧瓶(橡胶管已被弹簧夹夹紧),烧瓶内气体受热膨胀,使集气瓶中气体压强增大,在玻璃管中形成一段水柱,说明装置气密性良好,不漏气,故B正确;
C.装置②X若为CCl4,NH3或HCl极易溶于水且不溶于CCl4的气体,可以用装置③并可防倒吸,故C正确;
D.铁生锈过程中,如果空气参加反应,则瓶内气体压强减小,小于大气压,则导致U型管内液面“左高右低”,故D正确;
故选A.
点评:本题考查实验方案的设计,明确常见实验基本操作及钢铁的吸氧腐蚀和析氢腐蚀是解答本题的关键,注意设计实验应排除干扰,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法错误的是( )
| A、在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 |
| B、人们常采用牺牲阳极保护法防止通讯电缆发生腐蚀 |
| C、在电镀槽中,镀件做阴极,阳极选用镀层金属 |
| D、用惰性电极电解某硫酸铜溶液一段时间后,要恢复溶液的成分和浓度,可向溶液中加入一定量的氧化铜 |
研究者预想合成一个纯粹由氮组成的新物种N5+N3-,若N5+离子中每个氮原子均满足8电子结构,以下有关N5+推测正确的是( )
| A、N5+有24个电子 |
| B、N5+离子中存在三对未成键的电子对 |
| C、N5+阳离子中存在两个氮氮三键 |
| D、N5+在水中可以稳定存在 |
如图所示对实验Ⅰ~Ⅳ的实验现象预测正确的是( )
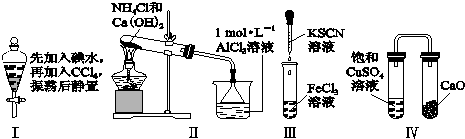

| A、实验Ⅰ:液体分层,下层呈无色 |
| B、实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C、实验Ⅲ:试管中立刻出现红色沉淀 |
| D、实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
下表是某矿物质饮用水的部分标签说明,则该饮用水中还可能较大量存在的离子是( )
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
主要成分 钾离子(K+):20^27.3mg/L 氯离子(Cl-):30^34.2mg/L 镁离子(Mg2+):20.2^24.9mg/L 硫酸根离子(SO42-):24^27.5mg/L.
| A、Ca2+ |
| B、Na+ |
| C、OH- |
| D、Ag+ |
化学与生产、生活、社会密切相关.下列有关说法错误的是( )
| A、松花蛋是一种常用食品,食用时有氨的气味,可以蘸些食醋除去 |
| B、“皮革奶”是奶粉中掺入皮革下脚料,将皮革灼烧时有烧焦羽毛的气味 |
| C、腌制食品中应严格控制NaNO2的用量 |
| D、从海水中可提取Mg,用惰性电极电解熔融的MgCl2或其水溶液都可制得Mg |
常温时,将500mLpH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法不正确的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a)g CuO |
| B、b<a<7 |
| C、阳极电极反应:4OH--4e-═2O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |
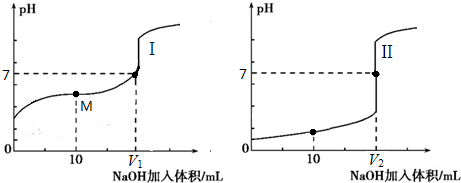 电解质的水溶液中存在电离平衡.
电解质的水溶液中存在电离平衡.