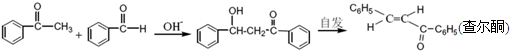
题目内容
在25℃时,某稀溶液中由水电离产生的c(H+)=10-13mol/L.有关该溶液的叙述正确的是( )
| A、该溶液的pH值可能为1 |
| B、水的电离受到促进 |
| C、水的离子积将变小 |
| D、该溶液的pH值一定为13 |
考点:弱电解质在水溶液中的电离平衡,水的电离
专题:电离平衡与溶液的pH专题
分析:在25℃时,某稀溶液中由水电离产生的c(H+)=10-13mol/L<10-7mol/L,说明该溶液中水的电离受到抑制,则溶液中的溶质为酸或碱,据此分析解答.
解答:
解:在25℃时,某稀溶液中由水电离产生的c(H+)=10-13mol/L<10-7mol/L,说明该溶液中水的电离受到抑制,则溶液中的溶质为酸或碱,
A.如果溶质是酸,则溶液的pH=1,如果是碱,溶液中的氢离子等于水电离出的氢离子,所以溶液的pH=13,故A正确;
B.某稀溶液中由水电离产生的c(H+)=10-13mol/L<10-7mol/L,说明该溶液中水的电离受到抑制,故B错误;
C.离子积常数只与温度有关,温度不变,水的离子积常数不变,故C错误;
D.根据A知,该溶液的pH可能是1或13,故D错误;
故选A.
A.如果溶质是酸,则溶液的pH=1,如果是碱,溶液中的氢离子等于水电离出的氢离子,所以溶液的pH=13,故A正确;
B.某稀溶液中由水电离产生的c(H+)=10-13mol/L<10-7mol/L,说明该溶液中水的电离受到抑制,故B错误;
C.离子积常数只与温度有关,温度不变,水的离子积常数不变,故C错误;
D.根据A知,该溶液的pH可能是1或13,故D错误;
故选A.
点评:本题考查弱电解质的电离,根据水的电离程度确定溶液中的溶质,注意水的离子积常数只与温度有关,与溶液酸碱性或浓度无关,为易错点.

练习册系列答案
相关题目
下列实验能成功的是( )
| A、将乙酸和乙醇混合加热制乙酸乙酯 |
| B、苯和浓溴水反应制溴苯 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热 |
高铁酸盐在能源、环境保护等有着广泛的用途,可以用电解法制高铁酸盐(已知高铁酸盐在酸性条件下不稳定),总反应式为Fe+2H2O+2OH-
3H2↑+FeO42-.下列说法正确的是( )
| ||
| A、铁为阳极,H2SO4为电解液 |
| B、铁为阴极,浓NaOH为电解液 |
| C、阳极发生的电极反应为Fe+8OH--6e-═4H2O+FeO42- |
| D、铁失去3 mol电子可以在阴极得到33.6 L氢气 |
下列说法正确的是( )
| A、镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B、已知AgCl的Ksp=1.8×10-10、Ag2CrO4的Ksp=1.2×10-12,所以相同温度下AgCl的溶解度大于Ag2CrO4 |
| C、常温下,将pH=8的醋酸钠溶液稀释,溶液中所有离子浓度都减小 |
| D、反应3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)在室温下可自发进行,则该反应的△H<0 |
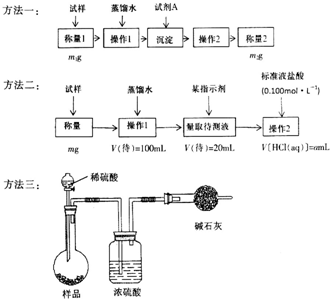 欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可采用以下四种方法.
欲测定含少量氯化钠的小苏打固态样品中NaHCO3的质量分数可采用以下四种方法.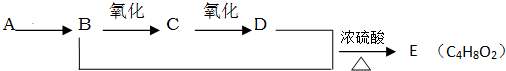
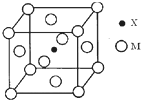 元素X基态原子的p电子比s电子少1个.元素Y基态原子的2p电子是2s电子的2倍.元素Z的一种单质为自然界硬度最大的物质.元素M位于第四周期,其基态原子失去3个电子后3d轨道半满.
元素X基态原子的p电子比s电子少1个.元素Y基态原子的2p电子是2s电子的2倍.元素Z的一种单质为自然界硬度最大的物质.元素M位于第四周期,其基态原子失去3个电子后3d轨道半满.