题目内容
实验室里制备Al(OH)3的方法最好的是( )
| A、在NaAlO2溶液中加入过量盐酸溶液 |
| B、在AlCl3溶液中加入过量氨水 |
| C、在AlCl3溶液中加入过量NaOH溶液 |
| D、用Al2O3与水反应 |
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:Al3+转化为不溶于水的物质是Al(OH)3,Al(OH)3具有两性,既能和酸反应又能和强碱反应,故用AlCl3制取Al(OH)3,选取试剂时不能选强碱,只能是弱碱.
解答:
解:A.在NaAlO2溶液中滴少量盐酸,反应H++AlO2-+H2O=Al(OH)3↓,生成氢氧化铝沉淀,加入过量盐酸溶液3H++Al(OH)3=Al3++3H2O,氢氧化铝沉淀溶解,故A错误;
B.氯化铝加入过量氨水生成氢氧化铝沉淀和氯化铵,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,氢氧化铝难溶于弱碱氨水,所以实验室里能用该法制备Al(OH)3,故B正确;
C.氯化铝溶液中加入氢氧化钠溶液先发生Al3++3OH-═Al(OH)3↓生成沉淀,后发生Al(OH)3+OH-═AlO2-+2H2O沉淀溶解,故先产生沉淀,后沉淀溶解,无法制得Al(OH)3,故C错误;
D.Al2O3与水不反应,无法制得Al(OH)3,故D错误;
故选B.
B.氯化铝加入过量氨水生成氢氧化铝沉淀和氯化铵,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,氢氧化铝难溶于弱碱氨水,所以实验室里能用该法制备Al(OH)3,故B正确;
C.氯化铝溶液中加入氢氧化钠溶液先发生Al3++3OH-═Al(OH)3↓生成沉淀,后发生Al(OH)3+OH-═AlO2-+2H2O沉淀溶解,故先产生沉淀,后沉淀溶解,无法制得Al(OH)3,故C错误;
D.Al2O3与水不反应,无法制得Al(OH)3,故D错误;
故选B.
点评:本题以氢氧化铝的制备为载体,考查铝的重要化合物的性质,难度不大,注意题目要求意在考查氢氧化铝的两性这一特性.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、0.1mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒 |
| B、2.8gN2和2.24 LCO组成的混合物中质子数为1.4 NA |
| C、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4+ |
| D、25℃时,1LpH=13的 Ba(OH)2溶液中含有的OH-数目为0.2 NA |
FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
| A、滴入盐酸,先产生沉淀,然后沉淀又溶解 |
| B、都能透过半透膜 |
| C、都有丁达尔现象 |
| D、都是均一的分散系 |
 科学家合成了一系列独特的氢铝化合物.最简单的氢铝化合物化学式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了一系列独特的氢铝化合物.最简单的氢铝化合物化学式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )| A、Al2H6中Al为-3价,H为+l价 |
| B、Al2H6在空气中完全燃烧,产物为氧化铝和水 |
| C、Al2H6是共价化合物 |
| D、氢铝化合物可能成为未来的储氢材料和火箭燃料 |
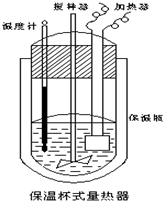 在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1.
在如图所示的量热计中,将100mL 0.50mol?L-1CH3COOH溶液与100mL0.55mol?L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J?℃-1生成溶液的比热容为4.184J?g-1?℃-1,溶液的密度均近似为1g?mL-1. 向Al2 (SO4)3逐滴加入NaOH溶液得到沉淀如图
向Al2 (SO4)3逐滴加入NaOH溶液得到沉淀如图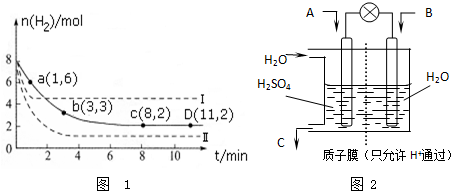
 如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题:
如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题: