题目内容
2.某固体粉末中可能含有SiO2、Na2O、Ca0、Cu0、Fe203,某同学设计并完成如下实验: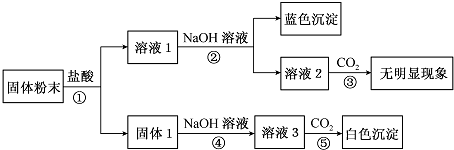
请回答:
(1)步骤②中生成蓝色沉淀的离子方程式为Cu2++2OH-=Cu(OH)2↓.
(2)步骤⑤中生成的白色沉淀是H2SiO3(填化学式).
(3)根据实验现象,固体粉末中一定存在的组分是SiO2、Cu0(填化学式).
分析 固体粉末中可能含有SiO2、Na2O、Ca0、Cu0、Fe203,加入盐酸,可以和盐酸反应的是Na2O、Ca0、Cu0、Fe203,SiO2和盐酸之间不反应,所以固体1是二氧化硅,可以和氢氧化钠之间反应得到硅酸钠溶液,向其中通入二氧化碳,可以得到硅酸白色沉淀,溶液1可以和氢氧化钠之间反应得到蓝色的氢氧化铜沉淀,所以固体中一定含有Cu0,一定不存在Fe203,溶液2中一定不含氢氧化钙,所以固体混合物一定不含Ca0,无法判断是否存在氧化钠.
解答 解:固体粉末中可能含有SiO2、Na2O、Ca0、Cu0、Fe203,加入盐酸,可以和盐酸反应的是Na2O、Ca0、Cu0、Fe203,SiO2和盐酸之间不反应,所以固体1是二氧化硅,可以和氢氧化钠之间反应得到硅酸钠溶液,向其中通入二氧化碳,可以得到硅酸白色沉淀,溶液1可以和氢氧化钠之间反应得到蓝色的氢氧化铜沉淀,所以固体中一定含有SiO2、Cu0,一定不存在Fe203,溶液2中一定不含氢氧化钙,所以固体混合物一定不含Ca0,无法判断是否存在氧化钠,综上分析得到:固体中一定含有SiO2、Cu0,一定不存在Ca0、Fe203,无法判断是否存在氧化钠.
(1)步骤②中生成蓝色沉淀的离子方程式为:Cu2++2OH-=Cu(OH)2↓,故答案为:Cu2++2OH-=Cu(OH)2↓;
(2)硅酸钠溶液中通入二氧化碳,可以得到硅酸白色沉淀,步骤⑤中生成的白色沉淀是硅酸H2SiO3,故答案为:H2SiO3;
(3)根据实验现象,固体粉末中一定存在的组分是SiO2、Cu0,故答案为:SiO2、Cu0.
点评 本题考查了物质检验方法的分析判断,物质性质的应用,掌握基础是关键注意物质和离子性质和反应现象的分析判断题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品.回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
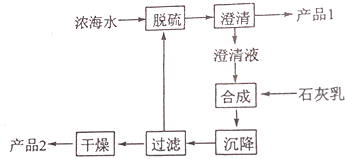
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的离子方程式为Ca2++SO42-=CaSO4↓,产品2的化学式为Mg(OH)2,1L浓海水最多可得到产品2的质量为69.6g.
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.

(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.
15.在下列条件下的离子组一定能够大量共存的是( )
| A. | 强碱性溶液中:K+、Mg2+、Cl-、SO42- | |
| B. | 含有大量H+的溶液中:Na+、Fe2+、NO3-、SO42- | |
| C. | 某无色溶液中:Na+、Al3+、Cl-、HCO3- | |
| D. | 常温下,由水电离出的c(H+)=1×10-12mol•L-1的无色溶液中:K+、Na+、Cl-、NO3- |
7.下列叙述中,正确的是( )
| A. | 氯化铝溶液中加入过量氨水反应的实质:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| B. | 在加入铝粉能放出氢气的溶液中,K+、NO3-、CO32-、Cl-一定能够大量共存 | |
| C. | 铁和稀HNO3反应后,溶液pH=2:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | 1 L0.1 mol•L-1FeCl3溶液和足量的Zn充分反应,生成11.2 g Fe |
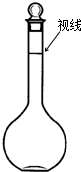 实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:
实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有: 草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用.
草酸(H2C2O4,二元酸弱)与草酸盐在实验和工业生产中都起着重要的作用. 如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题: