题目内容
15.在下列条件下的离子组一定能够大量共存的是( )| A. | 强碱性溶液中:K+、Mg2+、Cl-、SO42- | |
| B. | 含有大量H+的溶液中:Na+、Fe2+、NO3-、SO42- | |
| C. | 某无色溶液中:Na+、Al3+、Cl-、HCO3- | |
| D. | 常温下,由水电离出的c(H+)=1×10-12mol•L-1的无色溶液中:K+、Na+、Cl-、NO3- |
分析 A.生成氢氧化镁沉淀;
B.酸性条件下发生氧化还原反应;
C.发生互促水解反应的离子不能大量共存;
D.由水电离出的c(H+)=1×10-12mol•L-1的无色溶液,溶液可能呈酸性或碱性.
解答 解:A.碱性条件下Mg2+不能大量共存,生成氢氧化镁沉淀,故A错误;
B.酸性条件下Fe2+、NO3-发生氧化还原反应,不能大量共存,故B错误;
C.Al3+、HCO3-发生互促水解反应,不能大量共存,故C错误;
D.由水电离出的c(H+)=1×10-12mol•L-1的无色溶液,溶液可能呈酸性或碱性,无论酸性还是碱性,离子之间都不发生任何反应,可大量共存,故D正确.
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,注意选项B为解答的易错点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列有关说法正确的是( )
| A. | 分子晶体中共价键越强,熔沸点越高 | |
| B. | 只含共价键的物质,一定是共价化合物 | |
| C. | HF的分子间作用力大于HCl,故HF比HCl更稳定 | |
| D. | 分子晶体中,可能不存在共价键,但一定存在分子间作用力 |
6.下列有关Na+离子的叙述中正确的是( )
| A. | 有碱性 | B. | 有强氧化性 | C. | 有强还原性 | D. | 很难被还原 |
3.有关氨及氨水的说法,正确的是( )
| A. | NH3具有还原性 | B. | 液氨、氨气、氨水是同一种物质 | ||
| C. | 氨气是非电解质,氨水是电解质 | D. | 氨水的主要成分是NH3 |
10.某种不饱和烃分子中含有一个C≡C键、一个C═C键,催化加氢后的结构简式如下:(CH3CH2)2CHCH2CH(CH3)CH(CH3)2,则该烃的结构最多有( )
| A. | 3种 | B. | 6种 | C. | 7种 | D. | 10种 |
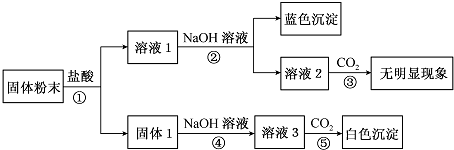
9.有一固体混合物,可能含有FeCl2?NaNO2?Ba(OH)2?AlCl3?Na2SO3中的若干种?取适量该混合物,加足量水充分搅拌,得到白色沉淀E与无色溶液G.继续进行以下实验:
①取少量E,加入稀硝酸直至过量,白色沉淀部分溶解;
②取少量G,逐滴加入稀硫酸直至过量,开始时不断生成白色沉淀后沉淀部分溶解;
③取少量G,滴加少量酸性高锰酸钾溶液,振荡,最终得无色溶液.
根据上述实验现象,以下推测不正确的是( )
①取少量E,加入稀硝酸直至过量,白色沉淀部分溶解;
②取少量G,逐滴加入稀硫酸直至过量,开始时不断生成白色沉淀后沉淀部分溶解;
③取少量G,滴加少量酸性高锰酸钾溶液,振荡,最终得无色溶液.
根据上述实验现象,以下推测不正确的是( )
| A. | 固体中无FeCl2 | B. | ③中使KMnO4褪色的是NO2- | ||
| C. | G的pH>7 | D. | 固体由Ba(OH)2?AlCl3?Na2SO3组成 |
7.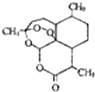 青蒿素是一种高效、速率搞疟药,是中医献给世界的一份礼物.其结构简式如图所示.下列有关青蒿素的说法正确的是( )
青蒿素是一种高效、速率搞疟药,是中医献给世界的一份礼物.其结构简式如图所示.下列有关青蒿素的说法正确的是( )
 青蒿素是一种高效、速率搞疟药,是中医献给世界的一份礼物.其结构简式如图所示.下列有关青蒿素的说法正确的是( )
青蒿素是一种高效、速率搞疟药,是中医献给世界的一份礼物.其结构简式如图所示.下列有关青蒿素的说法正确的是( )| A. | 易溶于乙醚等有机溶剂 | B. | 分子式为C15H21O5 | ||
| C. | 能在热的NaOH溶液中存在 | D. | 分子结构中含有极性键 |