题目内容
16.根据下列反应:(1)2Fe3++2I-═2Fe2++I2(2)Br2+2Fe2+═2Br-+2Fe3+ 判断下列顺序正确的是( )| A. | 还原性:Br->Fe2+>I- | B. | 还原性:I->Fe2+>Br- | ||
| C. | 氧化性:Br2>I2>Fe3+ | D. | 氧化性:I2>Fe3+>Br2 |
分析 根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性、还原剂的还原性大于还原产物的还原性来解答.
解答 解:2Fe3++2I-=2Fe2++I2中,I元素的化合价升高,Fe的化合价降低,则还原性I->Fe2+,氧化性:Fe3+>I2;
Br2+2Fe2+=2Fe3++2Br-中,Fe元素的化合价升高,Br的化合价降低,则还原性Fe2+>Br-,氧化性:Br2>Fe3+,
所以离子的还原性由强到弱的顺序为I->Fe2+>Br-,氧化性顺序为:Br2>Fe3+>I2;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及氧化还原反应中规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和标准状况下4.48L气体E,则E物质的摩尔质量为( )
| A. | 100g/mol | B. | 108g/mol | C. | 55g/mol | D. | 96g/mol |
4.工业上常用氯氧化法处理含氰(CN-)废水,反应原理为液氯在碱性条件下可以先将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一):KCN+2KOH+Cl2=KOCN+2KCl+H2O;氰酸盐再进一步被液氯氧化为无毒气体.下列说法不正确的是( )
| A. | KCN 与KOCN中氮元素的化合价均为-3价 | |
| B. | 氰酸盐被氧化过程中氮和碳的化合价均升高 | |
| C. | 氰酸盐进一步被氧化的产物之一是无毒的N2 | |
| D. | 完全处理含0.1 mol CN-的废水,理论上需要消耗Cl2的体积为5.6L(标准状况下) |
11.已知糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.请结合题意回答问题:
(1)燃料乙醇的生产过程可表示如下:玉米→粉碎→水解→发酵→过滤→a→乙醇
①粉碎玉米的目的是增大反应物的接触面积或加快反应速率或使反应充分进行.
②生产过程中若想证明淀粉部分水解的实验方法是取少许水解后的液体分别置于两试管中,一支加入氢氧化钠溶液使其pH大于7,再加入新制的氢氧化铜悬浊液,加热,产生砖红色沉淀,证明淀粉发生了水解,产生葡萄糖;另一支加入少量碘水,碘水变蓝,证明还有未水解的淀粉存在.
③步骤a的操作是C.
A.蒸发 B.萃取 C.蒸馏 D分液.
(2)除去下列物质中的少量杂质(括号内为杂质),试填下表
(3)根据三种营养物质的性质,判断下列说法正确的是B.
A.蔗糖和麦芽糖互为同分异构体,二者均能与银氨溶液反应,并且水解产物相同.
B.盐析可提纯蛋白质并保持其生理活性.
C.天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点.
D.两分子半胱氨酸(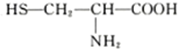 )脱水缩合形成二肽的结构简式为:
)脱水缩合形成二肽的结构简式为: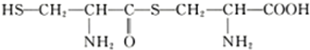 .
.
(4)写出工业上由硬脂酸甘油酯制肥皂的化学方程式: +3NaOH $\stackrel{加热}{→}$3C17H35COONa+
+3NaOH $\stackrel{加热}{→}$3C17H35COONa+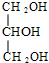 .
.
(1)燃料乙醇的生产过程可表示如下:玉米→粉碎→水解→发酵→过滤→a→乙醇
①粉碎玉米的目的是增大反应物的接触面积或加快反应速率或使反应充分进行.
②生产过程中若想证明淀粉部分水解的实验方法是取少许水解后的液体分别置于两试管中,一支加入氢氧化钠溶液使其pH大于7,再加入新制的氢氧化铜悬浊液,加热,产生砖红色沉淀,证明淀粉发生了水解,产生葡萄糖;另一支加入少量碘水,碘水变蓝,证明还有未水解的淀粉存在.
③步骤a的操作是C.
A.蒸发 B.萃取 C.蒸馏 D分液.
(2)除去下列物质中的少量杂质(括号内为杂质),试填下表
| 物质 | 加入试剂 | 去杂提纯方法 |
| 蛋白质(NaCl) | ||
| 肥皂(甘油) |
A.蔗糖和麦芽糖互为同分异构体,二者均能与银氨溶液反应,并且水解产物相同.
B.盐析可提纯蛋白质并保持其生理活性.
C.天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点.
D.两分子半胱氨酸(
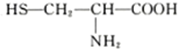 )脱水缩合形成二肽的结构简式为:
)脱水缩合形成二肽的结构简式为: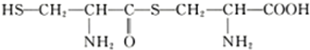 .
.(4)写出工业上由硬脂酸甘油酯制肥皂的化学方程式:
 +3NaOH $\stackrel{加热}{→}$3C17H35COONa+
+3NaOH $\stackrel{加热}{→}$3C17H35COONa+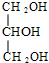 .
.  .
.

 .
. .
. .
. 、
、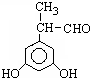 .
. (其中X、Y均部位H)
(其中X、Y均部位H)
 替代,请将Br2与Na2CO3反应的化学方程式补充完整
替代,请将Br2与Na2CO3反应的化学方程式补充完整