题目内容
1.在无色透明溶液中可以大量共存的离子组是( )| A. | H+ Na+ S2- CO32- | B. | H+ Ca2+ MnO${\;}_{4}^{-}$ NO${\;}_{3}^{-}$ | ||
| C. | K+ Ca2+ Cl- HCO${\;}_{3}^{-}$ | D. | Cl- Mg2+ Al3+ OH- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.氢离子与硫离子、碳酸根离子反应;
B.高锰酸根离子为有色离子;
C.四种离子之间不反应,都是无色离子;
D.镁离子、铝离子与氢氧根离子反应.
解答 解:无色溶液时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.H+与S2-、CO32-发生反应,在溶液中不能大量共存,故A错误;
B.MnO4-为有色离子,在溶液中不能大量存在,故B错误;
C.K+、Ca2+、Cl-、HCO3-之间不发生反应,都是无色离子,在溶液中能够大量共存,故C正确;
D.Mg2+、Al3+都与OH-发生反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
16.在10mL试管中集瞒了N02和N2的混合气体,把试管倒置在水槽中,水面上升,最后剩余6mL气体,由此可以说明( )
| A. | 原试管有4mL NO2 | B. | 6mL气体全部是N2 | ||
| C. | 原试管有6mL NO2 | D. | 剩余6mL气体是NO和N2的混合气体 |
16.2015年10月5日,中国女药学家屠呦呦与另外两位科学家共享2015年诺贝尔生理学或医学奖.屠呦呦因发现冶疗疟疾新型药物青蒿素和双氢青蒿素而获奖.青蒿素的分子式为C15H22O5.下列有关说法中正确的是( )

| A. | 青蒿素中氧元素的质量为80g | B. | 双氢青蒿素能发生酯化反应 | ||
| C. | 双氢青蒿素能与溴水发生加成反应 | D. | 青蒿素和双氢青蒿素均含羟基 |
6.下列关于物质的检验方法正确的是( )
| A. | 向某无色溶液中滴加氯化钡溶液,产生白色沉淀,再加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO42- | |
| B. | 某溶液能使淀粉碘化钾溶液变蓝,则该溶液一定为氯水或者溴水 | |
| C. | 向某白色固体粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原固体粉末中一定含CO32-或HCO3- | |
| D. | 将某白色固体粉末与氢氧化钠浓溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,证明原固体中一定含有NH4+ |
13.下列物质的用途中,不正确的是( )
| A. | 硅酸钠:木材防火剂 | B. | 二氧化硅:太阳能电池板 | ||
| C. | 过氧化钠:供氧剂 | D. | 小苏打:发酵粉主要成份 |
10.常温下,下列各溶液中微粒的物质的量浓度关系正确的是( )
| A. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa混合液,溶液显酸性,则溶液中粒子浓度:c(CH3COOH)>c(CH3COO-)>c (Na+)>c(H+)>c(OH-) | |
| B. | 浓度均为0.1 mol•L-1的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3) | |
| C. | 将0.2mol•L-1的某一元酸HA溶液和0.1mol•L-1的NaOH溶液等体积混合后溶液的pH大于7,则反应后的混合液:2c(OH-)+c(A-)═2c(H+)+c(HA) | |
| D. | 某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)═c(OH-)+c(HA-)+c(A2-) |
11.下列装置或操作正确,且能达到目的是( )
| A. | 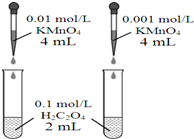 依据褪色快慢比较浓度对反应速率的影响 | |
| B. | 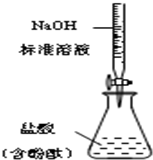 测定盐酸浓度 | |
| C. | 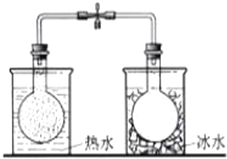 依据气体颜色变化,证明温度对平衡移动的影响 | |
| D. | 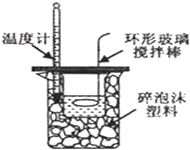 中和热的测定 |