题目内容
5.把NaHCO3和Na2CO3•10H2O混合物6.56g溶于水制成100mL溶液,其中c(Na+)=0.5mol•L-1.如果把6.56g这种混合物加热至恒重会失重多少克( )| A. | 2.65g | B. | 3.56g | C. | 3.91g | D. | 4.6g |
分析 NaHCO3和Na2CO3•10H2O混合物加热最终得到固体为Na2CO3,结合钠原子守恒计算.
解答 解:NaHCO3和Na2CO3•10H2O混合物加热最终得到固体为Na2CO3,混合物6.56g溶于水制成100mL溶液,其中c(Na+)=0.5mol•L-1,由Na原子守恒可知最终加热得到碳酸钠为0.1L×0.5mol/L×$\frac{1}{2}$×106g/mol=2.65g,则混合物加热至恒重会失重为6.56g-2.65g=3.91g,
故选C.
点评 本题考查混合物的计算,为高频考点,把握加热后的最终产物及原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
11.下列各组离子,能在溶液中大量共存的是( )
| A. | Fe2+.Na+.NO3-.H+ | B. | NH4+.Fe3+.SO42-.SCN- | ||
| C. | Ca2+.K+.CO32-.OH- | D. | SO42-.Cl-.Cu2+.Mg2+ |
9.下列实验能达到实验目的是( )
| A. | 将CuCl2溶液小心蒸干得到无水CuCl2 | |
| B. | 用AgNO3溶液鉴别NO2和Br2蒸气 | |
| C. | 电解熔融的AlCl3制备金属铝 | |
| D. | 用饱和Na2CO3溶液除去CO2气体中混有的HCl |
10.常温下,物质的量浓度均为0.1mol•L-1的下列溶液:①Na2CO3溶液 ②NaOH溶液 ③NaHSO4溶液 ④NH4Cl溶液 ⑤NaNO3,溶液的pH由小到大的排列顺序是( )
| A. | ③<④<⑤<①<② | B. | ④<③<⑤<①<② | C. | ④<③<①<⑤<② | D. | ①<④<③<⑤<② |
17.关于如图所示两个装置的叙述中不正确的是( )
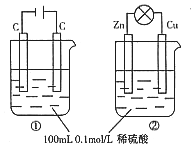

| A. | c(H+)浓度变化:①减小,②减小 | |
| B. | 装置名称:①是电解池,②是原电池 | |
| C. | 离子移动方向:①中H+向阴极方向移动,②中H+向正极方向移动 | |
| D. | 电极反应式:①中阳极:2H2O-4e-=4H++O2↑,②中负极:Zn-2e-=Zn2+ |
14.下列实验方法正确的是( )
| A. | 用分液漏斗分离乙酸和乙酸乙酯 | |
| B. | 用酚酞浓液鉴别未知浓度的NaOH溶液和Na2CO3溶液 | |
| C. | 用品红溶液鉴別SO2和CO2两种气体 | |
| D. | 用Ca(OH)2溶液鉴別Na2CO3 溶液和Na2HCO3溶液 |
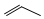
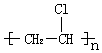 的单体是CH2=CHCl.
的单体是CH2=CHCl.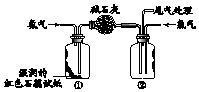 某同学利用图所示装置探究氨气的性质.
某同学利用图所示装置探究氨气的性质.