题目内容
9.下列实验能达到实验目的是( )| A. | 将CuCl2溶液小心蒸干得到无水CuCl2 | |
| B. | 用AgNO3溶液鉴别NO2和Br2蒸气 | |
| C. | 电解熔融的AlCl3制备金属铝 | |
| D. | 用饱和Na2CO3溶液除去CO2气体中混有的HCl |
分析 A.水解生成盐酸易挥发;
B.Br2蒸气与硝酸银反应生成浅黄色沉淀;
C.AlCl3为共价化合物,熔融状态不导电;
D.二者均与碳酸钠溶液反应.
解答 解:A.水解生成盐酸易挥发,蒸干得到氢氧化铜,故A错误;
B.Br2蒸气与硝酸银反应生成浅黄色沉淀,NO2不能,现象不同,可鉴别,故B正确;
C.AlCl3为共价化合物,熔融状态不导电,应电解熔融氧化铝制备Al,故C错误;
D.二者均与碳酸钠溶液反应,不能除杂,应选饱和碳酸氢钠溶液,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握盐类水解、物质鉴别、金属冶炼、混合物分离提纯、实验技能为解本题关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
20.实验是化学中最为重要的一部分,那么请问,下列说法正确的是( )
| A. | 称取10.1gNaOH时,将10g的砝码放在右盘,并将游码移到0.1g的位置 | |
| B. | 用试纸检验气体时,必须将湿润的试纸沾在玻璃棒上伸向气体 | |
| C. | 用剩的药品能否放回原瓶,应视具体情况而定 | |
| D. | 将铂丝放在稀硫酸中洗涤并灼烧后,再蘸取待检物进行焰色反应 |
17.一定条件下,一种反应物过量,另一种反应物可以完全反应的是( )
| A. | 过量的氧气与二氧化硫 | B. | 过量的氢氧化钠与二氧化硅 | ||
| C. | 过量的二氧化锰与浓盐酸 | D. | 过量的铜与浓硫酸 |
4.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.下列说法错误的是( )
| A. | 硫元素既被氧化,又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为2:1 | |
| C. | 相同条件下,每吸收10m3SO2就会放出2.5m3CO2 | |
| D. | 若生成2.24 L CO2,则转移0.8 mol电子 |
14.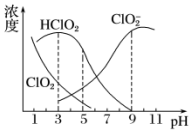 亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )
亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )
 亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )
亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | 25℃时,HClO2的电离平衡常数的数值Ka约为10-6 | |
| C. | 使用该漂白剂的最佳pH为3 | |
| D. | ClO2可用于自来水的消毒 |
5.把NaHCO3和Na2CO3•10H2O混合物6.56g溶于水制成100mL溶液,其中c(Na+)=0.5mol•L-1.如果把6.56g这种混合物加热至恒重会失重多少克( )
| A. | 2.65g | B. | 3.56g | C. | 3.91g | D. | 4.6g |
2.下列化学用语正确的是( )
| A. | HF的电子式:H+[:tr | |
| B. | Cl-离子的结构示意图: | |
| C. | 乙酸的结构简式:C2H3O2 | |
| D. | 硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
3.下列说法不正确的是( )
| A. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 与铜质水龙头的钢质水管,在连接处易发生腐蚀 | |
| D. | 大量燃烧化石燃料是造成雾霾的重要因素之一 |