题目内容
16.N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1,N2H4(g)+O2(g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1,则2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)的△H是( )| A. | -1 135.7 kJ•mol-1 | B. | 601.7 kJ•mol-1 | ||
| C. | -466.3 kJ•mol-1 | D. | 1 000.3 kJ•mol-1 |
分析 ①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1,②N2H4(g)+O2(g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1,则将方程式2×②-①得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g),依据盖斯定律计算反应热.
解答 解:①N2(g)+2O2(g)═2NO2(g)△H1=+67.7kJ•mol-1,②N2H4(g)+O2(g)═N2(g)+2H2O(g)△H2=-534kJ•mol-1,则将方程式2×②-①得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g),△H,依据盖斯定律:△H=2×△H2-△H1=2×(-534kJ•mol-1)-67.7kJ•mol-1=-1 135.7 kJ•mol-1,
故选:A.
点评 本题考查反应热的计算,掌握盖斯定律及其计算方法是关键,题目较简单.

练习册系列答案
相关题目
7.有四种有机物A、B、C、D,其分子式均为C3H6O2,把它们分别进行实验并记录现象如表:
四种物质的结构简式为:
A.CH3CH2COOH;B.CH3CHOHCHO;C.HCOOCH2CH3;D.CH3COOCH3.
| 有机物 | 氢氧化钠 | 银氨溶液 | 新制氢氧化铜 | 金属钠 |
| A | 发生中和反应 | 不反应 | 溶解 | 放出氢气 |
| B | 不反应 | 发生银镜反应 | 生成红色沉淀 | 放出氢气 |
| C | 不反应 | 发生银镜反应 | 生成红色沉淀 | 不反应 |
| D | 发生水解反应 | 不反应 | 不反应 | 不反应 |
A.CH3CH2COOH;B.CH3CHOHCHO;C.HCOOCH2CH3;D.CH3COOCH3.
4.能用于鉴别Na2CO3固体和NaHCO3固体的方法是( )
| A. | 加稀盐酸 | B. | 加NaOH溶液 | C. | 焰色反应 | D. | 加热 |
11.下列反应中必须加入氧化剂才能进行的是( )
| A. | SO32-→SO42- | B. | CO32-→CO2 | C. | Fe3+→Fe2+ | D. | MnO4-→Mn2+ |
1.下列说法啊正确的为( )
①植物油和裂化汽油都可以使溴水褪色
②煤经过气化、液化等物理变化可以得到清洁燃料
③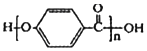 的结构中含有酯基
的结构中含有酯基
④1摩尔葡萄糖可以水解生成2摩尔乳酸(C3H6O3)
⑤聚合物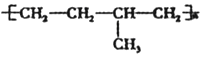 可由单体CH3-CH=CH2 和CH2=CH2加聚制得
可由单体CH3-CH=CH2 和CH2=CH2加聚制得
⑥煤含有苯、甲苯、二甲苯等有机物,可以用干馏方法获得苯.
①植物油和裂化汽油都可以使溴水褪色
②煤经过气化、液化等物理变化可以得到清洁燃料
③
 的结构中含有酯基
的结构中含有酯基④1摩尔葡萄糖可以水解生成2摩尔乳酸(C3H6O3)
⑤聚合物
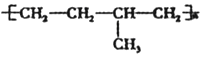 可由单体CH3-CH=CH2 和CH2=CH2加聚制得
可由单体CH3-CH=CH2 和CH2=CH2加聚制得⑥煤含有苯、甲苯、二甲苯等有机物,可以用干馏方法获得苯.
| A. | ①③⑤ | B. | ①②⑤ | C. | ②④⑤ | D. | ②③④ |
8.图为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题.
(1)在元素①~⑧中,金属性最强的元素是Na(填元素符号),最不容易形成化合物的元素是Ar(填元素符号).
(2)用电子式表示⑦的气态氢化物的形成过程 .
.
(3)③、④、⑥中原子半径由大到小的顺序是Na>S>F(填元素符号)
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)用电子式表示⑦的气态氢化物的形成过程
 .
.(3)③、④、⑥中原子半径由大到小的顺序是Na>S>F(填元素符号)
5.观察如图,下列叙述中错误的是( )


| A. | 图示实验中发生了化学变化 | |
| B. | 液体X的pH>7,液体Y是一种黑色黏稠状液体 | |
| C. | 气体Z易燃,可还原CuO | |
| D. | 液体Y是一种纯净物 |
