题目内容
市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol?L-1的Na2S2O3溶液20.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是 .
②根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg.
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
(2)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol?L-1的Na2S2O3溶液20.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是
②根据以上实验和包装袋说明,所测精制盐的碘含量是
考点:氧化还原反应方程式的配平,化学方程式的有关计算
专题:计算题,氧化还原反应专题
分析:(1)依据氧化还原反应的元素化合价变化升低相同,结合质量守恒配平;
(2)①溶液呈蓝色,随反应I2+2S2O32-=2I-+S4O62-进行,溶液中没有碘,溶液由蓝色为无色;
③根据I原子守恒找出碘酸钾中碘原子与碘单质的关系式分析计算;
(2)①溶液呈蓝色,随反应I2+2S2O32-=2I-+S4O62-进行,溶液中没有碘,溶液由蓝色为无色;
③根据I原子守恒找出碘酸钾中碘原子与碘单质的关系式分析计算;
解答:
解:(1)该反应中化合价的变化为:KIO3→I2,I元素由+5价→0价,一个KIO3分子得5个电子;KI→I2,I元素由-1价→0价,一个KI分子失一个电子,所以得失电子的最小公倍数为5,KIO3的计量数为1,KI的计量数为5,其它元素根据原子守恒配平,所以反应方程式为KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,
故答案为:1;5;3;3;3;3;
(2)①碘遇淀粉变蓝色,所以溶液呈蓝色,随反应I2+2S2O32-=2I-+S4O62-进行,溶液中没有碘,溶液由蓝色为无色,说明反应到终点,
故答案为:溶液由蓝色恰好变为无色;
②由 KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O32-=2I-+S4O62得,
I~3I2 ~6S2O32
127g 6mol
m(I) 6.0×10-4mol/L×0.02L
解得:m(I)=2.54×10-4g=2.54×10-1mg,
设每千克食盐中含碘xmg,列比例式为
=
,x=20,
故答案为:20;
故答案为:1;5;3;3;3;3;
(2)①碘遇淀粉变蓝色,所以溶液呈蓝色,随反应I2+2S2O32-=2I-+S4O62-进行,溶液中没有碘,溶液由蓝色为无色,说明反应到终点,
故答案为:溶液由蓝色恰好变为无色;
②由 KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O32-=2I-+S4O62得,
I~3I2 ~6S2O32
127g 6mol
m(I) 6.0×10-4mol/L×0.02L
解得:m(I)=2.54×10-4g=2.54×10-1mg,
设每千克食盐中含碘xmg,列比例式为
| 2.54×10-1mg |
| 12.7×10-3kg |
| xmg |
| 1kg |
故答案为:20;
点评:本题考查了氧化还原反应方程式的配平及有关计算,需要注意的是求食盐中碘的含量不是碘酸钾的含量,为易错点,题目难度中等.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
下列实验现象预测正确的是( )
A、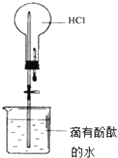 打开止水夹,烧瓶内出现红色喷泉 |
B、 酸性KMnO4溶液中出现气泡,颜色无明显变化 |
C、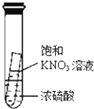 静置一段时间,小试管内有晶体析出 |
D、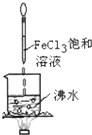 烧杯中液体变为红褐色后,继续加热煮沸,会出现浑浊 |
金属铜制取硝酸铜,从节约原料和防止环境污染考虑,最好的方法是( )
A、铜
| ||||
B、铜
| ||||
C、铜
| ||||
D、铜
|
关于居室内空气污染的说法错误的是( )
| A、居室内空气中存在的污染物主要来自于装修材料、日用化学品、香烟烟雾以及家用燃料的燃烧产物等 |
| B、燃料不完全燃烧产生的一氧化碳也是一种室内污染物 |
| C、在居室内放置几盒花草就可消除室内空气污染 |
| D、预防装修污染,最重要的是选择经过严格检测的、环保的装修材料 |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、X与Y形成的化合物中,X可以显负价,Y显正价 |
| B、最高正化合价:X大于Y |
| C、第一电离能可能Y小于X |
| D、气态氢化物的稳定性:HmY小于HnX |
20g密度为dg/cm3的硝酸钙溶液中,含有lgCa2+,则NO3-的物质的量浓度为( )
| A、mol/L |
| B、mol/L |
| C、2.5dmol/L |
| D、1.25dmol/L |
2molA与2molB混合于2L的密闭容器中,发生如下反应:2A(g)+3B(g)2C(g)+zD(g),若2s后,A的转化率为50%,测得v(D)=0.25mol?L-1?s-1,下列推断正确的是( )
| A、v(C)=v(A)=0.2 mol?L-1?s-1 |
| B、z=3 |
| C、B的转化率为75% |
| D、反应前与2 s后容器的压强比为4:3 |