题目内容
关于图的原电池,下列说法不正确的是( )
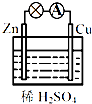

| A、能将化学能转变为电能 |
| B、锌电极上发生还原反应 |
| C、电子由锌片通过导线流向铜片 |
| D、铜电极上发生的电极反应为:2H++2e-=H2↑ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应;电子从负极沿导线流向正极;原电池中化学能转化为电能.
解答:
解:A、Zn、Cu、硫酸构成原电池,实现了化学能转化为电能,故A正确;
B、锌、铜和稀硫酸组成的原电池中,锌比铜活泼,Zn作负极,发生氧化反应,故B错误;
C、锌、铜和稀硫酸组成的原电池中,锌作负极,铜作正极,电子从负极沿导线流向正极,即电子由锌片通过导线流向铜片,故C正确;
D、锌、铜和稀硫酸组成的原电池中,铜作正极,正极上氢离子得电子发生还原反应为2H++2e-=H2↑,故D正确;
故选B.
B、锌、铜和稀硫酸组成的原电池中,锌比铜活泼,Zn作负极,发生氧化反应,故B错误;
C、锌、铜和稀硫酸组成的原电池中,锌作负极,铜作正极,电子从负极沿导线流向正极,即电子由锌片通过导线流向铜片,故C正确;
D、锌、铜和稀硫酸组成的原电池中,铜作正极,正极上氢离子得电子发生还原反应为2H++2e-=H2↑,故D正确;
故选B.
点评:本题考查学生原电池的工作原理,注意把握正负极的判断、电极方程式的书写、电子流向等,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A、pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol?L-1 |
| B、NaHCO3溶液中:c (H+)+c (H2CO3)=c(OH-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、17g的OH- 离子中含有的电子数为9NA |
| B、常温常压下,18 g H2O 中含有的原子总数为3NA |
| C、1mo1?L-1的A1C13溶液中,C1-离子的数目为3 NA |
| D、2.24 L四氯化碳分子中含有的分子数0.1NA |
下列有关物质应用的叙述中,不正确的是( )
| A、少量Cl2用于饮用水消毒 |
| B、氧化铝用于制造耐火材料 |
| C、Na2O2用于呼吸面具中供氧 |
| D、Si用于制造光导纤维 |
下列各组物质均由一种干燥气体和一种液体组成,其中可以进行喷泉实验,且液体几乎充满烧瓶的组合是( )
| A、Cl2,饱和食盐水 |
| B、SO2 氨水 |
| C、NH3,稀盐酸 |
| D、NO2水 |
用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、1mol/L的CaCl2溶液中含Cl-的数目为2NA |
| B、标准状况下,22.4LCl2和H2混合气体原子数为2NA |
| C、0.1mol AlCl3完全转化为氢氧化铝胶体,会生成0.1NA个胶粒 |
| D、常温常压下,100g 17% H2O2水溶液含氧原子总数为NA |
下列关于钠的说法正确的是( )
| A、金属钠与少量氧气反应生成氧化钠,与足量氧气反应生成过氧化钠 |
| B、钠的化学性质活泼,可从CuSO4溶液中置换出Cu |
| C、钠着火时可以用沙土盖灭 |
| D、钠在空气中燃烧,产生黄色火花 |
既能用浓H2SO4干燥,又能用P2O5干燥的气体是( )
| A、SO2 |
| B、H2S |
| C、NH3 |
| D、Cl2 |