题目内容
写出下列化学方程式、离子方程式或电离方程式:
(1)碳酸钠溶液和过量的醋酸溶液反应(离子方程式)
(2)镁在二氧化碳气体中燃烧(化学方程式)
(3)次氯酸电离(电离方程式)
(4)碳酸氢钠溶液和少量的澄清石灰水(离子方程式) .
(1)碳酸钠溶液和过量的醋酸溶液反应(离子方程式)
(2)镁在二氧化碳气体中燃烧(化学方程式)
(3)次氯酸电离(电离方程式)
(4)碳酸氢钠溶液和少量的澄清石灰水(离子方程式)
考点:离子方程式的书写,电离方程式的书写
专题:离子反应专题
分析:(1)碳酸钠溶液和过量的醋酸溶液反应生成醋酸钠和二氧化碳、水;
(2)镁在二氧化碳气体中燃烧生成氧化镁和碳;
(3)次氯酸为弱电解质,部分电离;
(4)碳酸氢钠溶液和少量的澄清石灰水反应生成碳酸钙、氢氧化钠和水.
(2)镁在二氧化碳气体中燃烧生成氧化镁和碳;
(3)次氯酸为弱电解质,部分电离;
(4)碳酸氢钠溶液和少量的澄清石灰水反应生成碳酸钙、氢氧化钠和水.
解答:
解:(1)碳酸钠溶液和过量的醋酸溶液反应,离子方程式为:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
故答案为:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
(2)镁在二氧化碳气体中燃烧化学方程式:2Mg+CO2
2MgO+C;
故答案为:2Mg+CO2
2MgO+C;
(3)次氯酸电离方程式为:HClO?H++ClO-;
故答案为:HClO?H++ClO-;
(4)碳酸氢钠溶液和少量的澄清石灰水,离子方程式:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-;
故答案为:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-;
故答案为:CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
(2)镁在二氧化碳气体中燃烧化学方程式:2Mg+CO2
| ||
故答案为:2Mg+CO2
| ||
(3)次氯酸电离方程式为:HClO?H++ClO-;
故答案为:HClO?H++ClO-;
(4)碳酸氢钠溶液和少量的澄清石灰水,离子方程式:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-;
故答案为:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-;
点评:本题考查了离子方程式、化学方程式的书写,明确物质的性质和发生反应的实质是解题关键,注意反应物用量对反应的影响,(4)为易错选项.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
2008年北京奥运会的“祥云”火炬所用的燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
| A、丙烷的分子式是C3H8 |
| B、丙烷分子中的碳原子在一条直线上 |
| C、丙烷在光照条件下能够发生取代反应 |
| D、丙烷的熔点比乙烷低 |
关于图的原电池,下列说法不正确的是( )
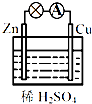

| A、能将化学能转变为电能 |
| B、锌电极上发生还原反应 |
| C、电子由锌片通过导线流向铜片 |
| D、铜电极上发生的电极反应为:2H++2e-=H2↑ |
在标准状况下,若VLH2S中含有的氢原子个数为n,则阿伏加德罗常数可表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法中正确的是( )
| A、摩尔是物质的质量的单位 |
| B、摩尔是一种基本物理量 |
| C、物质的量是一种基本物理量 |
| D、摩尔是指含有微粒数的多少 |
分类是化学学习与研究的常用方法,下列分类或说法正确的是( )
| A、Na2O、MgO、Al2O3均属于碱性氧化物 |
| B、根据纯净物的元素组成,将纯净物分为单质和化合物 |
| C、酸、碱、盐之间发生的反应一定属于复分解反应 |
| D、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
如图是某同学设计的储气装置(固定装置已略去),下列说法中,不正确的是( )


| A、打开止水夹a、b,气体从d管导入,储存在下面的集气瓶里 |
| B、取用储存在下面集气瓶里的气体时,通过控制止水夹a、b |
| C、气体被储存在下面的集气瓶里时,c导管也必须安装止水夹 |
| D、该装置也可作为制取二氧化碳气体的发生装置 |
现有盐酸、氯化钠、氢氧化钠和氯水四种溶液,可用来区别他们的一种试剂是( )
| A、AgNO3 |
| B、酚酞试剂 |
| C、紫色石蕊溶液 |
| D、饱和食盐水 |
金属晶体具有延展性的原因是( )


| A、金属键很微弱 |
| B、金属键没有饱和性 |
| C、密堆积层的阳离子容易发生滑动,但不会破坏密堆积的排列方式,也不会破坏金属键 |
| D、金属阳离子之间存在斥力 |