题目内容
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ |
| C、由C(石墨)=C(金刚石)△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| D、在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ?mol-1 |
考点:中和热,燃烧热
专题:
分析:A、等物质的量的硫蒸汽的能量比固体硫的能量高;
B、浓硫酸溶于水放热;
C、物质具有的能量越低越稳定;
D、氢气燃烧放热要与氢气的量成比例.
B、浓硫酸溶于水放热;
C、物质具有的能量越低越稳定;
D、氢气燃烧放热要与氢气的量成比例.
解答:
解:A、等物质的量的硫蒸气的能量高于硫固体的能量,对于放热反应,当产物相同时,反应物的能量越高,放出的热量越多,故前者放出的热量多,故A错误;
B、中和热是强酸强碱的稀溶液反应生成1mol水时放出的热量,浓硫酸溶于水放热,将含1molNaOH的溶液和含0.5molH2SO4的浓硫酸混合,放出的热量大于57.3 kJ,故B正确;
C、由C(石墨)→C(金刚石)△H=+1.90 kJ?mol-1可知,石墨能量低,石墨比金刚石稳定,故C错误;
D、在101kpa时,2gH2完全燃烧,生成液态水,放出285.8KJ热量,则氢气燃烧的热化学方程式表示为:H2(g)+
O2(g)═H2O(l)△H=-285.8KJ/mol,故D错误.
故选:B.
B、中和热是强酸强碱的稀溶液反应生成1mol水时放出的热量,浓硫酸溶于水放热,将含1molNaOH的溶液和含0.5molH2SO4的浓硫酸混合,放出的热量大于57.3 kJ,故B正确;
C、由C(石墨)→C(金刚石)△H=+1.90 kJ?mol-1可知,石墨能量低,石墨比金刚石稳定,故C错误;
D、在101kpa时,2gH2完全燃烧,生成液态水,放出285.8KJ热量,则氢气燃烧的热化学方程式表示为:H2(g)+
| 1 |
| 2 |
故选:B.
点评:本题考查了反应热量变化,热化学方程式的正误判断,物质能量与稳定性的比较方法,题目难度中等.

练习册系列答案
相关题目
我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与四氧化三铁发生铝热反应进行焊接而成的.下列有关该反应的说法中正确的是( )
| A、每生成1mol铁,转移电子3mol |
| B、Al被还原 |
| C、Fe3O4发生氧化反应 |
| D、Al是还原剂 |
下列离子方程式书写正确的是( )
| A、将少量SO2气体通入NaClO溶液中 SO2+2ClO-+H2O=SO32-+2HClO |
| B、向KHSO4溶液中加入Ba(OH)2溶液至所得溶液的pH=7 Ba2++OH-+H++SO42-=BaSO4↓+2H2O |
| C、向Ca(H2PO4)2溶液中滴入过量的NaOH溶液 3Ca2++6H2PO4-+12OH-=Ca3(PO4)2↓+4PO43-+12H2O |
| D、112mL(标况)Cl2通入10mL1mol/L的FeBr2溶液中 2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
用H2O2和H2SO4的混合溶液可溶解废旧印刷电路板上的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ?mol -11H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ?mol -1H2(g)+
O2(g)═H2O(l))△H=-285.84kJ?mol -1在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热△H等于( )
| 1 |
| 2 |
| A、-417.91kJ?mol -1 |
| B、-319.68kJ?mol -1 |
| C、+546.69kJ?mol -1 |
| D、-448.46kJ?mol -1 |
下列实验装置图正确的是( )
A、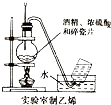 |
B、 |
C、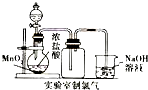 |
D、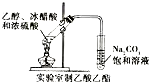 |
近日来,全国安全事故频发,折射出人们对化学品与安全知识的极度缺乏,下列有关化学品与安全的说法或操作错误的是( )
A、运石油的油罐车上应贴  标志,装运浓硫酸的槽罐车应贴 标志,装运浓硫酸的槽罐车应贴  标志,并由专人押运 标志,并由专人押运 |
| B、欲往燃烧的酒精炉中添加酒精必须要先熄灭酒精炉并等酒精炉完全冷却后才能加入酒精 |
| C、炒菜时油锅着火,立即加水灭火;电器起火时,应立即切断电源并采取适当措施灭火 |
| D、若家中出现煤气泄露,会闻到浓烈的气味,应马上开窗通风,切不可打电话或打开其他电器. |
热还原法冶炼金属的反应一定是( )
| A、置换反应 | B、分解反应 |
| C、复分解反应 | D、氧化还原反应 |