题目内容
下列实验装置图正确的是( )
A、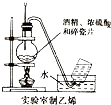 |
B、 |
C、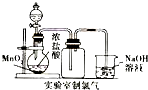 |
D、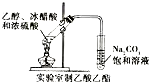 |
考点:化学实验方案的评价
专题:
分析:A.温度计测量溶液温度,制取的乙烯中含有乙醇蒸气;
B.实验室制氨气是利用氯化铵和氢氧化钙加热反应,氨气比空气轻;
C.浓盐酸和二氧化锰需要加热才能反应;
D.乙酸和碳酸钠反应生成可溶性醋酸钠、乙醇极易溶于水,乙酸乙酯不易溶于碳酸钠溶液.
B.实验室制氨气是利用氯化铵和氢氧化钙加热反应,氨气比空气轻;
C.浓盐酸和二氧化锰需要加热才能反应;
D.乙酸和碳酸钠反应生成可溶性醋酸钠、乙醇极易溶于水,乙酸乙酯不易溶于碳酸钠溶液.
解答:
解:A.温度计应该测量溶液温度而不是蒸气温度,乙醇易挥发,制取的乙烯中含有乙醇蒸气,所以收集乙烯前要出去乙醇,故A错误;
B.固体固体加热制氨气,发生装置符合,氨气比空气轻,用向下拍空气法收集,收集装置符合,故B正确;
C.实验室制氯气二氧化锰和浓盐酸需要加热才能反应,故C错误;
D.乙酸和碳酸钠反应生成可溶性醋酸钠、乙醇极易溶于水,导管不能插入液面以下,以免发生倒吸,故D错误.
故选B.
B.固体固体加热制氨气,发生装置符合,氨气比空气轻,用向下拍空气法收集,收集装置符合,故B正确;
C.实验室制氯气二氧化锰和浓盐酸需要加热才能反应,故C错误;
D.乙酸和碳酸钠反应生成可溶性醋酸钠、乙醇极易溶于水,导管不能插入液面以下,以免发生倒吸,故D错误.
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质制备及气体收集等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
相关题目
在使溶液中的AlO2-完全转化成Al(OH)3,应选择的最好试剂是( )
| A、H2SO4 |
| B、HCl |
| C、CO2 |
| D、NH3?H2O |
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉质量相等,则原溶液中H+和Cl-的物质的量之比为( )
| A、1:4 | B、1:7 |
| C、1:8 | D、2:5 |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ |
| C、由C(石墨)=C(金刚石)△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| D、在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ?mol-1 |
已知反应:①101kPa时,2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
又知由H2和O2两种气体反应生成1mol液态水比生成1mol气态水多放出44kJ热量.下列结论中正确的是( )
| A、H2的燃烧热为285.8 kJ/mol | ||
B、H2和O2反应生成液态水时的热化学方程式为H2(g)+
| ||
| C、稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ | ||
| D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
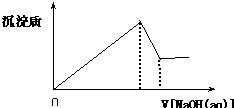 向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )
向某溶液中逐滴加入0.5mol/L的NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则该溶液中可能存在的离子是( )| A、只有Mg2+ |
| B、只有Al3+ |
| C、有H+、Mg2+和Al3+ |
| D、有Mg2+和Al3+ |
下列有关物质的量的理解正确的是( )
| A、物质的量和摩尔是两个不同的物理量 |
| B、摩尔是物质的量的单位,1摩尔任何物质含6.02x1023个原子 |
| C、阿伏伽德罗常数是人们规定的数,没有单位 |
| D、当H2的摩尔质量以g.mol-1为单位时,在数值上与H2的相对分子质量相等 |