题目内容
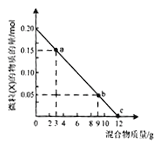
【题目】室温下向10mL 0.1 molL﹣1NaOH溶液中加入0.1molL﹣1的一元酸HA溶液pH的变化曲线如图所示.下列说法正确的是( ) 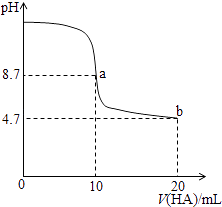
A.a点所示溶液中c(Na+)>c(A﹣)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A﹣)+c(HA)
D.b点所示溶液中c(A﹣)>c(HA)
【答案】D
【解析】 解:A.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性,应为c(HA)>c(H+),故A错误;
B.a点A﹣水解,促进水的电离,b点时HA过量,溶液呈酸性,HA电离出H+ , 抑制水的电离,故B错误;
C.pH=7时,c(H+)=c(OH﹣),由电荷守恒可知c(Na+)+c(H+)=c(A﹣)+c(OH﹣),则c(Na+)=c(A﹣),故C错误;
D.b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA电离程度大于A﹣水解程度,则存在c(A﹣)>c(HA),故D正确.
故选D.
A.a点时酸碱恰好中和,溶液pH=8.7,说明HA为弱酸,NaA溶液水解呈碱性;
B.b点时HA过量,溶液呈酸性,HA电离出H+ , 抑制水的电离; C.pH=7时,c(H+)=c(OH﹣),结合电荷守恒判断;D.b点HA过量一倍,溶液存在NaA和HA,溶液呈酸性,说明HA电离程度大于A﹣水解程度.

 综合自测系列答案
综合自测系列答案【题目】教材中用酸性KMnO4溶液和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如图一和表: 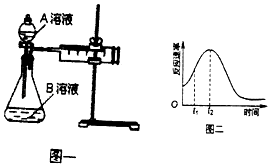
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 molL﹣1H2C2O4溶液 | 30 mL 0.01 molL﹣1kMnO4溶液 |
② | 20 mL 0.2 molL﹣1 | 30 mL 0.01 molL﹣1KMnO4溶液 |
(1)用电离方程式表示草酸溶液显酸性的原因
(2)该实验探究的是因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是①②(填“>”“<”“=”)
(3)若实验①在2min末收集了896mL CO2(标准状况下),则用MnO4﹣表示该时间内的化学反应速率为v (MnO4﹣)= .
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定来比较化学反应速率.
(5)该实验小组同学发现反应速率如图二所示,其中t1~t2时间内速率变快的主要原因可能是:①该反应放热、② .
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
B | 向无色溶液中加硝酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中一定含SO |
C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
D | 向某溶液中先加氯水再加KSCN溶液 | 溶液呈血红色 | 原溶液中一定含Fe2+ |
A. A B. B C. C D. D