题目内容
16.设NA为阿伏加德罗常数的值.下列叙述正确的是( )| A. | 标准状况下,11.2LSO3所含的氧原子数为1.5NA | |
| B. | 常温常压下,7.8gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA | |
| C. | 电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA | |
| D. | 500ml 1mol/L醋酸溶液中含氧原子数为NA |
分析 A、标况下三氧化硫为固体;
B、过氧化钠和硫化钠的摩尔质量均为78g/mol,且均由2个钠离子和1个阴离子构成,且阴离子过氧根和硫离子中含有的电子数均为18个;
C、电解精炼铜时,阳极上放电的不只是铜,还有比铜活泼的金属;
D、醋酸溶液中除了醋酸分子外,水也含氧原子.
解答 解:A、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、过氧化钠和硫化钠的摩尔质量均为78g/mol,故7.8g混合物的物质的量为0.1mol,且两者均由2个钠离子和1个阴离子构成,故0.1mol混合物中含有的阴离子个数为0.1NA个,而两者中的阴离子过氧根和硫离子中含有的电子数均为18个,故0.1NA个阴离子中含有的电子的个数为1.8NA个,故B正确;
C、电解精炼铜时,阳极上放电的不只是铜,还有比铜活泼的金属,故当阳极质量减少6.4g时,转移的电子数多于0.2NA个,故C错误;
D、醋酸溶液中除了醋酸分子外,水也含氧原子,故溶液中的氧原子的个数多于NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
11.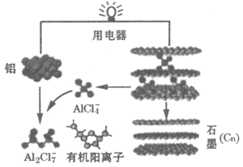 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 放电时,有机阳离子向铝电极方向移动 | |
| C. | 放电时的负极反应为:Al-3e-+7AlCl4-═4Al2Cl7- | |
| D. | 充电时,AlCl4-向石墨电极方向移动 |
4.已知H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)↓+2H2O(l)△H=-1 584.2kJ•mol-1;HCl(aq)与NaOH(aq)反应的中和热△H=-55.6kJ•mol-1.则生成SO42-(aq)+Ba2+(aq)=BaSO4(s)的反应热等于( )
| A. | -1 528.6 kJ•mol-1 | B. | -1 473 kJ•mol-1 | ||
| C. | +1 473 kJ•mol-1 | D. | +1 528.6 kJ•mol-1 |
8.0.5L Cl-为3mol/L的 FeCl3溶液的物质的量浓度为( )
| A. | 3 mol/L | B. | 1.5 mol/L | C. | 1 mol/L | D. | 0.5 mol/L |
5.只能表示一个化学反应的离子方程式是( )
| A. | Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | CO32-+2H+=H2O+CO2↑ | |
| C. | 2Br-+Cl2=2Cl-+Br2 | |
| D. | SO2+Cl2+2H2O=4H++2Cl-+SO42- |
6.氯仿(CHCl3,非电解质)在空气中能发生缓慢氧化,生成剧毒物质光气(COCl2,非电解质),化学方程式为2CHCl3+O2═2COCl2+2HCl.检验氯仿是否被氧化应选用的试剂是( )
| A. | 水 | B. | 硝酸酸化的硝酸银溶液 | ||
| C. | 酚酞溶液 | D. | 氢氧化钠溶液 |