题目内容
如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )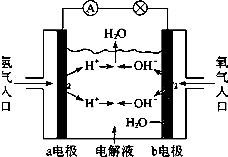

| A、a电极是负极 |
| B、电子从b电极流向a电极 |
| C、在电池工作中,a电极附近pH值降低 |
| D、b电极的电极反应为:4OH--4e-═2H2O+O2↑ |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:氢氧燃料电池中,氢气易失电子发生氧化反应,所以通入氢气的电极是负极,氧气易得电子发生还原反应,所以通入氧气的电极是正极;当电解质溶液是强碱时,负极上氢气失电子和氢氧根离子反应生成水,正极上氧气得电子生成氢氧根离子;当电解质溶液是酸时,负极上氢气生成氢离子,正极上氧气和氢离子反应生成水.
解答:
解:A.燃料电池中,通入燃料氢气的电极a是负极,所以a电极是负极,故A正确;
B.燃料电池中电子从负极流向正极,则从a极流向b极,故B错误;
C.在电池工作中,a电极上氢气失电子生成氢离子,所以a电极附近pH值降低,故C正确;
D.b电极为正极,正极上氧气得电子发生还原反应,则正极的电极反应式为:O2+4e-+2H2O═4OH-或O2+4e-+4OH-═2H2O,故D错误;
故选BD.
B.燃料电池中电子从负极流向正极,则从a极流向b极,故B错误;
C.在电池工作中,a电极上氢气失电子生成氢离子,所以a电极附近pH值降低,故C正确;
D.b电极为正极,正极上氧气得电子发生还原反应,则正极的电极反应式为:O2+4e-+2H2O═4OH-或O2+4e-+4OH-═2H2O,故D错误;
故选BD.
点评:本题考查了燃料电池,要注意的是:虽然燃料相同,但电解质溶液不同时,电极反应式就不同,如氢氧燃料电池,在酸性介质和碱性介质中的电极反应式就不同,题目难度不大.

练习册系列答案
相关题目
下列物质既能与盐酸反应,又能与NaOH 溶液反应的是( )
| A、KHCO3 |
| B、NaOH |
| C、KAl(SO4)2 |
| D、Cu(NO3)2 |
一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:CH4(g)+4NO(g)?2N2(g)+CO2(g)+2H2O(g)△H=-1160.0kJ?mol-1 H2O(l)=H2O(g)△H=+44.0kJ?mol-1 若取一定量的CH4和NO投入到恒容的密闭容器中,下列有关说法正确的是( )
| A、当该反应体系平均分子质量不变时,反应体系达到平衡 |
| B、当容器中每生成1 mol H2O(1)时,放出的能量为536.0kJ |
| C、升高温度,正反应速率加快,平衡常数减小 |
| D、加入高效催化剂可以一定程度上提高NO转化率 |
将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).判断该分解反应已经达到化学平衡的是( )
| A、2v(NH3)=v(CO2) |
| B、密闭容器中c(NH3):c(CO2)=2:1 |
| C、密闭容器中混合气体的密度不变 |
| D、密闭容器中氨气的体积分数不变 |
下列实验操作或结论正确的是( )
| A、配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水 |
| B、实验室里需要480 mL 2.0 mol?L-1的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作 |
| C、25℃时,用惰性电极电解某浓度的NaOH溶液,一小段时间后,NaOH溶液的浓度可能增大,也可能不变 |
| D、实验室配制500 mL 0.2 mol/L的硫酸亚铁溶液,其操作是:用天平称27.8 g绿矾,放入500 mL容量瓶,加水溶解、稀释、定容、摇匀 |
下列过程属于熵增加的是( )
| A、一定条件下,水由气态变成液态 |
| B、Ag+(aq)+Cl-(aq)=AgCl(s) |
| C、4NO2(g)+O2(g)═2N2O5 (g) |
| D、火柴盒中的火柴散落到地上 |
分子式为C4H9Cl的同分异构体共有( )种.(不考虑立体异构)
| A、4种 | B、8种 | C、2种 | D、3种 |
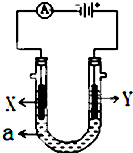 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: