题目内容
将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).判断该分解反应已经达到化学平衡的是( )
| A、2v(NH3)=v(CO2) |
| B、密闭容器中c(NH3):c(CO2)=2:1 |
| C、密闭容器中混合气体的密度不变 |
| D、密闭容器中氨气的体积分数不变 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、未体现正逆的关系,故A错误;
B、只要反应发生,密闭容器中就存在c(NH3):c(CO2)=2:1,故B错误;
C、密闭容器中混合气体的密度不变,说明气体质量不变,正逆反应速率相等,故C正确;
D、从反应开始到平衡,密闭容器中氨气的体积分数不变一直不变,故D错误;
故选C.
B、只要反应发生,密闭容器中就存在c(NH3):c(CO2)=2:1,故B错误;
C、密闭容器中混合气体的密度不变,说明气体质量不变,正逆反应速率相等,故C正确;
D、从反应开始到平衡,密闭容器中氨气的体积分数不变一直不变,故D错误;
故选C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列关于常见有机化合物的说法中,正确的是( )
| A、蛋白质、葡萄糖和乙酸均属电解质 |
| B、甲烷和苯都能发生氧化反应和取代反应 |
| C、乙醇和乙酸分子中都含羟基,都能与NaOH发生反应 |
| D、糖类、油脂和蛋白质都是人体必需的营养物质,它们的组成元素相同 |
从海水中提取溴常用的一种工艺涉及以下过程:则正确的步骤为( )
①氧化:用Cl2将海水中的NaBr氧化成Br2;
②将海水浓缩;
③提取:用Cl2将HBr氧化成Br2得到产品;
④富集:用空气和水蒸气将Br2吹入吸收塔与吸收剂SO2水溶液反应生成HBr.
①氧化:用Cl2将海水中的NaBr氧化成Br2;
②将海水浓缩;
③提取:用Cl2将HBr氧化成Br2得到产品;
④富集:用空气和水蒸气将Br2吹入吸收塔与吸收剂SO2水溶液反应生成HBr.
| A、②①③④ | B、①②③④ |
| C、③②①④ | D、②①④③ |
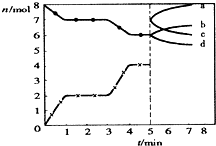 高温下进行反应:C(s)+CO2(g)?2CO(g)△H=xkJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图:下列说法正确的是( )
高温下进行反应:C(s)+CO2(g)?2CO(g)△H=xkJ/mol.如图为CO2、CO的物质的量n随时间t的变化关系图:下列说法正确的是( )A、2min时,
| ||||
| B、0~lmin,v(CO)=1 mol/(L?min);1~3min时,v(CO)=v(CO2) | ||||
| C、3min时温度由T1升高到T2,则x>O | ||||
| D、5min时再充入一定量的CO,a、d曲线分别表示n(CO)、n(CO2)的变化 |
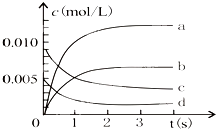 在2L恒容密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变 化如下表则下列判断正确的是( )
在2L恒容密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变 化如下表则下列判断正确的是( )| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO) (mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| A、平衡时NO的转化率是3.5% |
| B、右图中表示NO2变化的曲线是a |
| C、容器内气体的密度保持不变能说明该反应已达到平衡状态 |
| D、当v逆 (NO)=2v正(O2) 时能说明该反应已达到平衡状态 |
如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )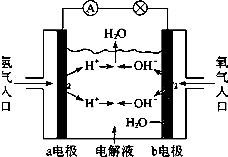

| A、a电极是负极 |
| B、电子从b电极流向a电极 |
| C、在电池工作中,a电极附近pH值降低 |
| D、b电极的电极反应为:4OH--4e-═2H2O+O2↑ |
下列说法正确的是( )
| A、摩尔是物质的数量单位 |
| B、58.5gNaCl溶解在1L水中,得到溶液的物质的量浓度为1mol/L |
| C、标况下,1molCCl4所占的体积约为22.4L |
| D、12g12C含有的碳原子数约为6.02×1023个 |