题目内容
6.下列有关物质性质的比较顺序中,不正确的是( )| A. | 热稳定性:HF<HCl<HBr<HI | B. | 微粒半径:K+>Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 熔点:Li>Na>K>Rb |
分析 A.非金属性越强,对应氢化物的稳定性越强;
B.电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小;
C.非金属性越强,对应最高价含氧酸的酸性越强;
D.碱金属的离子半径越大,金属键越弱,熔点越低.
解答 解:A.非金属性越强,对应氢化物的稳定性越强,则热稳定性:HF>HCl>HBr>HI,故A错误;
B.电子层越多,离子半径越大,具有相同电子排布的离子中原子序数大的离子半径小,则微粒半径:K+>Na+>Mg2+>Al3+,故B正确;
C.非金属性越强,对应最高价含氧酸的酸性越强,则酸性:HClO4>H2SO4>H3PO4>H2SiO3,故C正确;
D.碱金属的离子半径越大,金属键越弱,熔点越低,熔点:Li>Na>K>Rb,故D正确;
故选A.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
16.下列分离或提纯物质的说法正确的是( )
| A. | 过滤,可以除去NaCl溶液中少量的淀粉胶体 | |
| B. | 溶解、过滤,可以提纯含少量BaSO4的BaCO3 | |
| C. | 加热蒸发,可以除去粗盐中的CaCl2、MgCl2等杂质 | |
| D. | 加入足量铁屑,充分反应后,过滤,可以除去FeCl2溶液中少量FeCl3 |
17.由气体发生装置导出的气体是甲烷、一氧化碳、氢气中的一种,下列推断正确的是( )
| A. | 将气体通入高锰酸钾酸性溶液和溴水,溶液颜色无变化,该气体一定是甲烷 | |
| B. | 在导管口点燃该气体,火焰呈淡蓝色,用内壁涂有澄清石灰水的烧杯罩在火焰上方,烧杯壁上有白色物质产生,该气体一定是甲烷 | |
| C. | 在导管口点燃该气体,火焰呈淡蓝色,用干燥的冷烧杯罩在火焰上方,烧杯壁上有水珠产生,该气体一定是甲烷 | |
| D. | 若上述B和C的现象均能出现,则可判断该气体一定是甲烷 |
14.下列反应中,属于取代反应的是( )
| A. | 实验室制取乙烯 | |
| B. | 乙酸与乙醇在浓硫酸和加热条件下的酯化反应 | |
| C. | 葡萄糖与银氨溶液反应 | |
| D. | 乙醛和氢气的反应 |
1.下列说法正确的是( )
①淀粉、纤维素、油脂、蛋白质都是天然有机高分子化合物
②淀粉、纤维素、蔗糖都属于糖类
③三大营养素糖类、油脂、蛋白质中,油脂是热能最高的营养素
④用纯碱( Na2CO3)热溶液洗涤餐具上的油污
⑤氯水使红墨水褪色原理和CH2=CH2使Br2的CCl4溶液褪色原理相同
⑥现用清洁燃料主要有压缩天然气和液化石油气两类,它们均属于碳氢化合物.
①淀粉、纤维素、油脂、蛋白质都是天然有机高分子化合物
②淀粉、纤维素、蔗糖都属于糖类
③三大营养素糖类、油脂、蛋白质中,油脂是热能最高的营养素
④用纯碱( Na2CO3)热溶液洗涤餐具上的油污
⑤氯水使红墨水褪色原理和CH2=CH2使Br2的CCl4溶液褪色原理相同
⑥现用清洁燃料主要有压缩天然气和液化石油气两类,它们均属于碳氢化合物.
| A. | ①②③ | B. | ②③④⑥ | C. | ②④⑤⑥ | D. | ③④⑤ |
18.下列各组物质的溶液,不加任何其他试剂,就能将其一一区别出来的是( )
| A. | NaCl、Na2CO3、Ba(NO3)2、H2SO4 | B. | BaCl2、CuSO4、NaOH、NaCl | ||
| C. | NaCl、NaOH、H2SO4、Ba(NO3)2 | D. | K2SO4、BaCl2、K2CO3、KNO3 |
15.95℃时水的离子积约为KW=1.0×10-12,pH=8的CH3COONa溶液中,由水电离出的OH-浓度是( )
| A. | 1×10-10mol•L-1 | B. | 1×10-8mol•L-1 | C. | 1×10-4mol•L-1 | D. | 1×10-6mol•L-1 |
9.食品香精菠萝酯的生产路线(反应条件略去)如下:
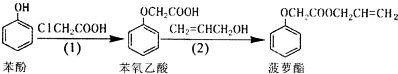
下列叙述错误的是( )

下列叙述错误的是( )
| A. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)中由苯酚生成苯氧乙酸的反应属于取代反应 | |
| D. | 可用溴水检验步骤(2)的产物中是否有烯丙醇(CH2=CHCH2OH) 残留 |