题目内容
5.有四位同学分别对四种溶液中所含的离子进行检测,所得结果如下,其中所得结果错误的是( )| A. | Mg+、Na+、Cl-、NO3- | B. | Na+、NO3-、OH-、HCO3- | ||
| C. | OH-、CO32-、Cl-、K+ | D. | Ba2+、Na+、OH-、NO3- |
分析 A.四种离子之间不发生反应,可以共存于同一溶液;
B.氢氧根离子与碳酸氢根离子反应;
C.四种离子之间不反应,可以共存;
D.四种离子之间不发生反应,可以大量共存.
解答 解:A.Mg+、Na+、Cl-、NO3-之间不反应,可以共存于同一溶液,不满足题干要求,故A错误;
B.OH-、HCO3-之间发生反应,不可能共存于同一溶液,满足题干要求,故B正确;
C.OH-、CO32-、Cl-、K+之间不发生反应,可以共存于同一溶液,故C错误;
D.Ba2+、Na+、OH-、NO3-之间不满足离子反应发生条件,能够大量共存,故D错误;
故选B.
点评 本题考查了离子共存的判断,为高考高频题,题目难度中等,明确离子反应发生的条件为解答关键,试题侧重基础知识的考查,培养了学生的灵活运用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.向密闭容器中通入2体积SO2和1体积02,在一定条件下反应:2SO2+O2?2S03,达平衡.此时容器内硫原与氧原子数之比为1:3,则SO2的转化率为( )
| A. | 10% | B. | 50% | C. | 90% | D. | 无法计算 |
16.下列有机物同分异构体数目相同的是( )
| A. | 分子式为C4H8的烃与丙烷的二氯取代物 | |
| B. | 分子式为C5H12的烃与分子式为C2H4O2且能发生银镜反应的有机物 | |
| C. | 分子式都为C8H10O的醇和酚 | |
| D. | 甲苯的一氯取代物与分子式为C4H10O的醇 |
13.将下列各组物质按酸、碱、盐分类顺序排列,正确的是( )
| A. | H2SO4 Na2CO3 Ca(OH)2 | B. | HCl NaOH K2CO3 | ||
| C. | H2CO3 C2H5OH NaHSO4 | D. | Ba(OH)2 H3PO4 KOH |
20.实验室要配制1.0mol/L硫酸溶液500mL,需要用10mol/L的硫酸溶液的体积是( )
| A. | 25mL | B. | 250mL | C. | 50mL | D. | 500mL |
10.离子方程式正确的是( )
| A. | 过氧化钠加到冷水中:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 过量氢氧化钠溶液与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ | |
| C. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO${\;}_{2}^{-}$+H2O | |
| D. | 氢氧化钡溶液中加入稀硫酸:H++OH-═H2O |
17.乙苯催化脱氢制苯乙烯反应:
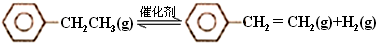
(1)已知:
计算上述反应的△H=+12 kJ•mol-1.
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$ (用α等符号表示).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和 水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如所示: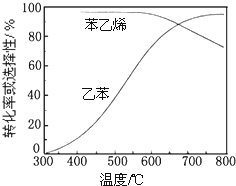
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工 艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平 衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用.

(1)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$ (用α等符号表示).
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和 水蒸气的物质的量之比为1:9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应.在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如所示:

①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实正反应为气体分子数增大的反应,保持压强不变,加入水蒸气,容器体积应增大,等效为降低压强,平衡向正反应方向移动.
②控制反应温度为600℃的理由是600℃时乙苯的转化率与苯乙烯的选择性均较高,温度过低,反应速率较慢,转化率较低,温度过高,选择性下降,高温下可能失催化剂失去活性,且消耗能量较大.
(4)某研究机构用CO2代替水蒸气开发了绿色化学合成工 艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯.保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:CO2+H2=CO+H2O,CO2+C=2CO.新工艺的特点有①②③④(填编号).
①CO2与H2反应,使乙苯脱氢反应的化学平 衡右移
②不用高温水蒸气,可降低能量消耗
③有利于减少积炭
④有利于CO2资源利用.
14.下列有关微粒或物质的“量”的叙述不正确的是( )
| A. | 浓度分别为2 mol/L和1 mol/L的Na2CO3溶液中,C(CO32一)的比值为2:1 | |
| B. | 常温常压下,16 g 02和O3混合气体中含有NA个氧原子 | |
| C. | 46 g NO2和N204混合气体的物质的量之和大于O.5 mol,小于l mol | |
| D. | 向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250 g |
15.设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A. | 0.5 mol锌粒与足量盐酸反应产生11.2 L H2 | |
| B. | 标准状况下,18g的H2O中含有的电子数为10NA | |
| C. | 常温常压下,11.2L氧气所含的原子数为NA | |
| D. | 2.4g金属镁变为镁离子失去的电子数为0.1NA |