题目内容
14.下列有关微粒或物质的“量”的叙述不正确的是( )| A. | 浓度分别为2 mol/L和1 mol/L的Na2CO3溶液中,C(CO32一)的比值为2:1 | |
| B. | 常温常压下,16 g 02和O3混合气体中含有NA个氧原子 | |
| C. | 46 g NO2和N204混合气体的物质的量之和大于O.5 mol,小于l mol | |
| D. | 向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250 g |
分析 A.碳酸钠是强碱弱酸盐,碳酸根离子水解,且其浓度越小水解程度越大;
B.氧气和臭氧中都只含有氧原子,16g二者的混合物中含有16g氧原子,含有1mol氧原子;
C.46g二氧化氮的物质的量为1mol,46g四氧化二氮的物质的量为0.5mol,则46g二者的混合物的物质的量介于二者之间;
D.硫酸铜固体与水结合生成五水硫酸铜,且饱和溶液中水减少,则会从溶液中析出硫酸铜.
解答 解:A.浓度分别为2mol/L和1mol/L的Na2CO3溶液中,碳酸根离子发生水解,且浓度不同,水解程度不同,则溶液中C(CO32-)的比值不是2:1,故A错误;
B.16g氧气和臭氧的混合物中含有16g氧原子,16g氧原子含有1mol,含有NA个氧原子,故B正确;
C.由于46gNO2的物质的量为1mol,46gN204的物质的量为0.5mol,则46gNO2和N204混合气体的物质的量之和大于O.5mol,小于lmol,故C正确;
D.1mol硫酸铜与水结合生成1mol五水硫酸铜,饱和溶液中水减少,则会析出部分晶体,所以析出的晶体的质量大于250g,故D正确;
故选A.
点评 本题考查了有关物质的量的计算、盐的水解原理,题目难度中等,注意掌握物质的量与摩尔质量等物理量之间的转化关系,明确盐的水解原理及其应用方法,选项BD为易错点,注意饱和溶液的特点.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
4.下列措施不利于改善环境质量的是( )
| A. | 在燃煤中添加石灰石粉末 | B. | 用中和法除去工业废水中的酸 | ||
| C. | 随意地堆放生活垃圾 | D. | 在汽车上按照汽车尾气净化器 |
5.有四位同学分别对四种溶液中所含的离子进行检测,所得结果如下,其中所得结果错误的是( )
| A. | Mg+、Na+、Cl-、NO3- | B. | Na+、NO3-、OH-、HCO3- | ||
| C. | OH-、CO32-、Cl-、K+ | D. | Ba2+、Na+、OH-、NO3- |
2.在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液生成沉淀的量与滴入NaOH溶液的体积关系如图所示则原混合溶液中Al2(S04)3与MgSO4中SO42-的物质的量浓度之比为( )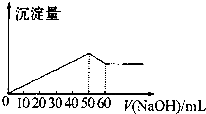

| A. | 6:1 | B. | 3:1 | C. | 3:4 | D. | 3:2 |
19.如图,有机化合物Ⅰ转化为Ⅱ的反应类型是( )
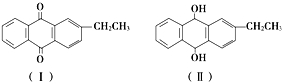

| A. | 氧化反应 | B. | 还原反应 | C. | 取代反应 | D. | 水解反应 |
6.有机物M是苯的同系物,其结构为 ,则M可能的结构简式共有( )
,则M可能的结构简式共有( )
 ,则M可能的结构简式共有( )
,则M可能的结构简式共有( )| A. | 6种 | B. | 12种 | C. | 24种 | D. | 32种 |
3.物质的量浓度都是0.1mol/L的下列溶液,酸性最强的是( )
| A. | HCl | B. | H2SO4 | C. | CH3COOH | D. | ( NH4)2SO4 |
4.下列行为中符合安全要求的是( )
| A. | 装运乙醇的包装箱上应贴上易燃液体的危险品标志图标 | |
| B. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| C. | 实验时,将水倒入浓硫酸中配制稀硫酸 | |
| D. | 进入煤矿井时,用火把照明 |