题目内容
如图是一套制取并验证氯气部分化学性质的实验装置,回答下列问题: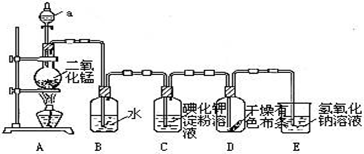
(1)装置A中反应的方程式为 ;
(2)仪器a的名称叫 ,该仪器中盛有的试剂为 ;
(3)当Cl2气流通过一段时间后,装置B中溶液的pH值 7(填“>”、“<”或“=”),写出Cl2与水反应的离子方程式 ;
(4)当有少量Cl2气流通过后,观察到装置C中的溶液变为 色,反应的离子方程式为 ;
(5)当Cl2气流持续通过时,装置D中干燥的有色布条 (填“能”或“不能”)褪色,原因是 ;
(6)装置E的作用是 .

(1)装置A中反应的方程式为
(2)仪器a的名称叫
(3)当Cl2气流通过一段时间后,装置B中溶液的pH值
(4)当有少量Cl2气流通过后,观察到装置C中的溶液变为
(5)当Cl2气流持续通过时,装置D中干燥的有色布条
(6)装置E的作用是
考点:氯气的实验室制法
专题:实验题
分析:(1)浓盐酸与二氧化锰在加热条件下反应生成氯化锰、氯气和水;
(2)熟悉常见仪器,知道其名称及用途;
(3)氯气与水反应生成氯化氢和次氯酸,氯化氢完全电离出氢离子和氯离子,次氯酸部分电离出氢离子和次氯酸根离子;
(4)氯气氧化碘离子为碘单质遇到淀粉变蓝;
(5)氯气不具有漂白性,具有漂白性的是次氯酸;
(6)氯气有毒,是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收.
(2)熟悉常见仪器,知道其名称及用途;
(3)氯气与水反应生成氯化氢和次氯酸,氯化氢完全电离出氢离子和氯离子,次氯酸部分电离出氢离子和次氯酸根离子;
(4)氯气氧化碘离子为碘单质遇到淀粉变蓝;
(5)氯气不具有漂白性,具有漂白性的是次氯酸;
(6)氯气有毒,是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收.
解答:
解:(1)浓盐酸与二氧化锰在加热条件下反应生成氯化锰、氯气和水,化学方程式为:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑;
故答案为:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑;
(2)仪器a为分液漏斗;用来盛放反应的浓盐酸,利用分液漏斗将浓盐酸滴入烧瓶中加热反应;
故答案为:分液漏斗,浓盐酸;
(3)氯气与水反应生成氯化氢和次氯酸,离子方程式为:Cl2+H2O?H++Cl-+HClO,氯化氢完全电离出氢离子和氯离子,次氯酸部分电离出氢离子和次氯酸根离子,溶液呈酸性pH<7;
故答案为:<;Cl2+H2O?H++Cl-+HClO;
(4)装置C中通过氯气会发生氧化还原反应,氯气氧化碘离子为碘单质,反应离子方程式为:Cl2+2I -=2Cl-+I2,碘单质遇到淀粉变蓝;
故答案为:蓝色;Cl2+2I -=2Cl-+I2;
(5)氯气不具有漂白性,具有漂白性的是次氯酸,所以D中干燥的有色布条不褪色;
故答案为:不能;氯气不具有漂白性;
(6)氯气有毒,是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收;
故答案为:吸收多余的氯气.
| ||
故答案为:MnO2+4HCl(浓)
| ||
(2)仪器a为分液漏斗;用来盛放反应的浓盐酸,利用分液漏斗将浓盐酸滴入烧瓶中加热反应;
故答案为:分液漏斗,浓盐酸;
(3)氯气与水反应生成氯化氢和次氯酸,离子方程式为:Cl2+H2O?H++Cl-+HClO,氯化氢完全电离出氢离子和氯离子,次氯酸部分电离出氢离子和次氯酸根离子,溶液呈酸性pH<7;
故答案为:<;Cl2+H2O?H++Cl-+HClO;
(4)装置C中通过氯气会发生氧化还原反应,氯气氧化碘离子为碘单质,反应离子方程式为:Cl2+2I -=2Cl-+I2,碘单质遇到淀粉变蓝;
故答案为:蓝色;Cl2+2I -=2Cl-+I2;
(5)氯气不具有漂白性,具有漂白性的是次氯酸,所以D中干燥的有色布条不褪色;
故答案为:不能;氯气不具有漂白性;
(6)氯气有毒,是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收;
故答案为:吸收多余的氯气.
点评:本题考查了氯气的制备和性质的检验,熟悉氯气的性质是解题关键,注意实验现象分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质中,不可用来漂白、杀菌消毒的是( )
| A、次氯酸钠 | B、过氧化钠 |
| C、氯水 | D、含碘食盐 |
等体积等浓度的MOH强碱溶液和HA弱酸溶液混和后,混和液中有关离子的浓度浓度应满足的关系是( )
| A、c(M+)>c(A-)>c( OH-)>c(H+) |
| B、c(M+)>c(A-)>c(H+)>c( OH-) |
| C、c(M+)>c( OH-)>c(A-)>c(H+) |
| D、c(M+)>c(H+)=c( OH-)>c(A-) |
下列说法不正确的是( )
| A、Ksp只与难溶电解质的性质和温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、任意两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
| D、t℃时,Ksp(CaCO3)=4×10-16,则CaCO3饱和溶液中c(Ca2+)=2×10-8 mol/L |
下列各式属于正确的水解反应的离子方程式的是( )
| A、HCO3-+H2O?CO32-+H3O+ |
| B、S2-+H2O?H2S+2OH- |
| C、Fe3++3H2O?Fe(OH)3+3H+ |
| D、CH3COOH+OH-?CH3COO-+H2O |
下列三种化合物由左到右是按强电解质、弱电解质、非电解质的顺序排列的一组是( )
| A、HCl、CaCO3、SO2 |
| B、KNO3、CH3COOH、NH3 |
| C、HClO、H2S、C2H5OH |
| D、BaSO4、H3PO4、H2O |