题目内容
下列说法不正确的是( )
| A、Ksp只与难溶电解质的性质和温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、任意两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
| D、t℃时,Ksp(CaCO3)=4×10-16,则CaCO3饱和溶液中c(Ca2+)=2×10-8 mol/L |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.化学反应平衡常数只与反应本身的性质和温度有关,与溶液中离子浓度无关;
B.从难溶电解质的溶解平衡的角度分析;
C.对于阴、阳离子的个数比相同即同一类型的难溶电解质,Ksp的数值越大,难溶电解质在水中的溶解能力越强即溶解度越大.对于阴、阳离子的个数比不同的难溶电解质,不能直接用Ksp的大小比较它们的溶解能力;
D.依据溶度积常数计算.
B.从难溶电解质的溶解平衡的角度分析;
C.对于阴、阳离子的个数比相同即同一类型的难溶电解质,Ksp的数值越大,难溶电解质在水中的溶解能力越强即溶解度越大.对于阴、阳离子的个数比不同的难溶电解质,不能直接用Ksp的大小比较它们的溶解能力;
D.依据溶度积常数计算.
解答:
解:A.化学反应平衡常数只与反应本身的性质和温度有关,当难溶物确定时就只和温度有关了,故A正确;
B.由于Ksp(ZnS)>Ksp(CuS),在ZnS饱和溶液中加入Cu2+溶液,可生成CuS沉淀,故B正确;
C.对于阴、阳离子的个数比相同即同一类型的难溶电解质,Ksp的数值越大,难溶电解质在水中的溶解能力越强即溶解度越大.对于阴、阳离子的个数比不同的难溶电解质,不能直接用Ksp的大小比较它们的溶解能力,必须通过计算进行比较,故C错误;
D.t℃时,Ksp(CaCO3)=c(Ca2+)c(CO32-)=4×10-16,CaCO3饱和溶液中c(Ca2+)c=(CO32-),计算得到,c(Ca2+)=2×10-8 mol/L,故D正确;
故选C.
B.由于Ksp(ZnS)>Ksp(CuS),在ZnS饱和溶液中加入Cu2+溶液,可生成CuS沉淀,故B正确;
C.对于阴、阳离子的个数比相同即同一类型的难溶电解质,Ksp的数值越大,难溶电解质在水中的溶解能力越强即溶解度越大.对于阴、阳离子的个数比不同的难溶电解质,不能直接用Ksp的大小比较它们的溶解能力,必须通过计算进行比较,故C错误;
D.t℃时,Ksp(CaCO3)=c(Ca2+)c(CO32-)=4×10-16,CaCO3饱和溶液中c(Ca2+)c=(CO32-),计算得到,c(Ca2+)=2×10-8 mol/L,故D正确;
故选C.
点评:本题考查难溶电解质的溶解平衡,侧重于平衡常数的含义与应用的理解,题目难度不大,注意不同类型的难溶物的化学计量数不同,它作为各离子浓度的次方数对Ksp的影响有很大差别.所以不能用这两种Ksp的相对大小来比较难溶物的溶解度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用下列实验装置进行相应实验,能达到实验目的是( )
A、 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 制取少量乙烯气体 |
C、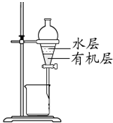 分离CCl4萃取溴水后已分层的有机层和水层 |
D、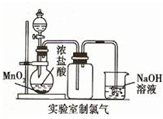 装置制取少量Cl2气体 |
在铁和铜的混合物中加入一定量的稀硝酸,充分反应后剩余金属的质量为m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属的质量为m2g,则m1与m2的关系是( )
| A、m1>m2 |
| B、m1≤m2 |
| C、m1≥m2 |
| D、m1=m2 |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是( )
| A、AgNO3 (Ag2O) |
| B、NaOH(NaOH) |
| C、NaCl (盐酸) |
| D、CuSO4(Cu(OH)2) |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7,c(SO42-)=c(NH4+) | ||
| B、两种醋酸溶液物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | ||
D、向0.1moL?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
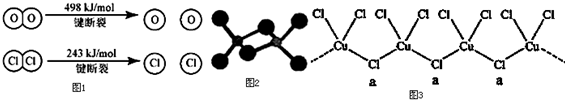
已知:①lmolH2分子中化学键断裂时需要吸收436kJ的能量②1mol C12分子中化学键断裂时需要吸收243kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431kJ的能量下列叙述中正确的是( )
| A、氢气和氯气反应生成氯化氢气体的热化学方程式是:H2(g)+Cl2(g)=2HCl(g)△H=366KJ?mol-1 |
| B、氢气和氯气反应生成2 mol氯化氢气体,反应的△H=366KJ?mol-1 |
| C、氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183KJ?mol-1 |
| D、氢气和氯气反应生成1 mol氯化氢气气体,反应的△H=-183KJ?mol-1 |