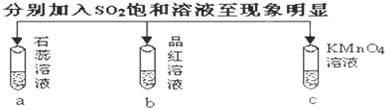
题目内容
19.由CO2、H2和CO组成的混合气体在同温、同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为( )| A. | 19:8:13 | B. | 22:1:14 | C. | 13:9:29 | D. | 26:16:27 |
分析 根据CO2、H2和CO碳组成的混合气体在同温、同压下与氮气的密度相同,可知混合气体的平均相对分子质量等于氮气的相对分子质量,即为28,而CO的相对分子质量也为28,则二氧化碳与氢气的平均相对分子质量必须为28,设出二氧化碳和氢气的体积,然后列式计算即可.
解答 解:CO2、H2和CO组成的混合气体在同温、同压下与N2的密度相同,则混合气体的平均相对分子质量等于氮气的相对分子质量,即为28,
由于CO的相对分子质量为28,则CO2和H2的平均相对分子质量为28即可,CO的体积不受限制,
设混合气体中CO2的体积为x,H2的体积为y,相同条件下气体体积之比等于物质的量之比,
则:$\frac{44x+2y}{x+y}$=28,整理可得:CO2和H2的体积之比=13:8,CO的体积为任意体积,选项中只有D符合,
故选D.
点评 本题考查物质的量的计算、混合物的计算,题目难度不大,明确相同条件下气体的密度之比等于相对分子质量之比计算即可,试题侧重于学生的分析能力和计算能力的考查.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
14.能使KMnO4酸性溶液褪色的物质是( )
| A. | 苯 | B. | 乙烷 | C. | 乙烯 | D. | 甲烷 |
4.下列有关氨和铵盐的说法正确的是( )
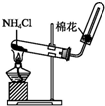

| A. | 氨和铵盐都易溶于水,都能生成NH4+ | |
| B. | 铵态氮肥与碱性物质如草木灰混合施用肥效更高 | |
| C. | 实验室制备氨气的试剂和装置可为如图装置 | |
| D. | 工业上用氨气液化需吸收热量的过程做制冷剂 |
11.检验牙膏中是否含有甘油选用的试剂是( )
| A. | 氢氧化钠溶液 | B. | 新制氢氧化铜浊液 | ||
| C. | 醋酸溶液 | D. | 碳酸钠溶液 |
14.下列关于某些物质(离子)的检验方法或结论正确的是( )
| A. | 用丁达尔效应鉴别NaCl溶液和KCl溶液 | |
| B. | 向某溶液中加入BaCl2溶液出现白色沉淀,则该溶液中肯定有SO42- | |
| C. | 用KSCN溶液鉴别FeCl2溶液和Fe2(SO4)3溶液 | |
| D. | 用焰色反应可鉴别出NaCl、KCl和Na2SO4三种物质 |
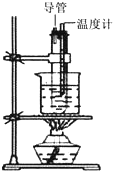 用苯和浓硝酸、浓硫酸按照如图装置制取硝基苯,回答下列问题:
用苯和浓硝酸、浓硫酸按照如图装置制取硝基苯,回答下列问题: ;反应类型:取代反应.
;反应类型:取代反应.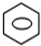 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$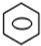 -NO2+H2O
-NO2+H2O ;
;