题目内容
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题(1)图中明显的两处错误是
①温度计的水银球未置于支管口处
②
(2)B仪器的名称是
(3)实验时A中除加入自来水外,加入沸石的作用是
考点:实验室制取蒸馏水
专题:
分析:(1)蒸馏时,要保证水充满冷凝管,冷凝水应从下口进入;
(2)根据的仪器的图形确定仪器的名称;
(3)蒸馏时,要加入碎瓷片,防止液体暴沸.
(2)根据的仪器的图形确定仪器的名称;
(3)蒸馏时,要加入碎瓷片,防止液体暴沸.
解答:
解:(1)冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,则图中的错误为冷却水的方向上进下出,
故答案为:冷却水的方向上进下出;
(2)由仪器的结构可知,A为蒸馏烧瓶,B为冷凝管,
故答案为:冷凝管;
(3)为防止液体暴沸,应加碎瓷片,若加热后发现未加沸石,应停止加热待装置冷却后加入沸石,水没冷却温度较高时不能加沸石,否则会产生爆沸;
故答案为:防止暴沸;停止加热待装置冷却后加入沸石.
故答案为:冷却水的方向上进下出;
(2)由仪器的结构可知,A为蒸馏烧瓶,B为冷凝管,
故答案为:冷凝管;
(3)为防止液体暴沸,应加碎瓷片,若加热后发现未加沸石,应停止加热待装置冷却后加入沸石,水没冷却温度较高时不能加沸石,否则会产生爆沸;
故答案为:防止暴沸;停止加热待装置冷却后加入沸石.
点评:本题考查实验室制备蒸馏水操作,题目难度不大,本题注意实验操作要点,学习中注意正确操作方法和实验的注意事项.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
水的电离平衡曲线如图所示,下列说法正确的是( )
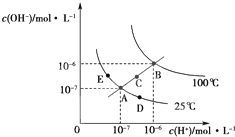

| A、图中五点KW间的关系:B=C=A=D=E |
| B、若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合,溶液显酸性 |
| C、若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
| D、若从A点到D点,可采用:温度不变在水中加入少量的酸 |
 可逆反应2X+Y?2Z在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(z)与反应时间(t)的关系如图所示.下列判断正确的是 ( )
可逆反应2X+Y?2Z在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(z)与反应时间(t)的关系如图所示.下列判断正确的是 ( )| A、T1<T2,P1<P2 |
| B、T1<T2,P1>P2 |
| C、T1>T2,P1>P2 |
| D、T1>T2,P1<P2 |
下列各组离子,在强碱性溶液中可以大量共存的是( )
| A、Na+、Br-、Cl-、S2- |
| B、Na+、K+、NH4+、Ba2+ |
| C、Ca2+、K+、Cl-、CO32- |
| D、SO32-、NO3-、SO42-、HCO3- |
能证明醋酸是一种弱酸的事实是( )
| A、醋酸溶液能跟钠反应放出H2 |
| B、1mol/L醋酸溶液的pH小于7 |
| C、1mol/L醋酸钠溶液的pH约为9 |
| D、pH=5醋酸稀释100倍后7>pH>5 |
某反应可以表示成mM+nH++O2=xM2++yH2O则x的值是( )
| A、2 | B、4 | C、6 | D、9 |