题目内容
 可逆反应2X+Y?2Z在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(z)与反应时间(t)的关系如图所示.下列判断正确的是 ( )
可逆反应2X+Y?2Z在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量n(z)与反应时间(t)的关系如图所示.下列判断正确的是 ( )| A、T1<T2,P1<P2 |
| B、T1<T2,P1>P2 |
| C、T1>T2,P1>P2 |
| D、T1>T2,P1<P2 |
考点:体积百分含量随温度、压强变化曲线
专题:
分析:根据温度、压强对平衡移动的影响分析,温度越高、压强越大,则反应速率越大,达到平衡用的时间越少,曲线的斜率越大,先拐先平温度、压强大.
解答:
解:根据温度对反应速率的影响可知,温度越高,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:T1>T2;
根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,先拐先平压强大,故有:P1>P2,
故选C.
根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,先拐先平压强大,故有:P1>P2,
故选C.
点评:本题考查化学平衡图象题,题目难度中等,注意温度、压强对反应速率和化学平衡的影响.

练习册系列答案
相关题目
恒温下将1molN2和3mol H2 在体积为2L的容器中混合,发生如下反应:N2(g)+3H2(g)?2NH3(g),2s后测得NH3的体积分数为25%,则下列说法中不正确的是( )
| A、用N2浓度的减少表示的平均反应速率为0.2mol?L-1?s-1 |
| B、2s时N2的转化率为40% |
| C、2s时混合气体中n(N2):n(H2):n(NH3)═3:9:4 |
| D、2s时NH3的浓度为0.4mol/L |
下列离子在水溶液中一定能大量共存的是( )
| A、Na+、NH4+、SO42-、Cl- |
| B、OH-、Na+、H+、SO42- |
| C、Mg2+、Cl-、Na+、OH- |
| D、CO32-、H+、SO42-、K+ |
常温下某强酸溶液pH=a,某强碱溶液pH=b,已知a+b=12,酸碱溶液混合后pH=7,则酸溶液体积V(酸)和碱溶液体积V(碱)的正确关系为( )
| A、V(碱)=V(酸) |
| B、V(碱)=10V(酸) |
| C、V(碱)=100V(酸) |
| D、V(碱)=1000V(酸) |
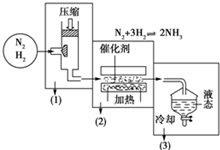 已知海水电解制得的氢气用于合成氨,某合成氨厂生产流程如图:
已知海水电解制得的氢气用于合成氨,某合成氨厂生产流程如图: 
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题