题目内容
14.下列离子方程式书写不正确的是( )| A. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | H2S的电离方程式为 H2S+H2O?HS-+H3O+ | |
| C. | 用铁做电极电解饱和食盐水的阳极反应式:Fe-2e-═Fe2+ | |
| D. | 用两个铜片作电极电解盐酸:Cu+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cu2+ |
分析 A.铝离子与生成的氢氧根离子结合生成氢氧化铝沉淀;
B.硫化氢为弱电解质,电离分步进行,主要以第一步为主;
C.阳极铁失去电子生成亚铁离子;
D.阳极铜放电,阴极氢离子得到电子生成氢气.
解答 解:A.用石墨作电极电解AlCl3溶液生成氢氧化铝、氢气、氯气,其离子反应为:2Al3++6Cl-+6H2O$\frac{\underline{\;电解\;}}{\;}$3Cl2↑+3H2↑+2Al(OH)3↓,故A错误;
B.H2S的电离分步进行,主要以第一步为主,其电离方程式为:H2S+H2O?HS-+H3O+,故B正确;
C.用铁做电极电解饱和食盐水,阳极Fe失去电子生成亚铁离子,其电极反应式为:Fe-2e-═Fe2+,故C正确;
D.用两个铜片作电极电解盐酸,阳极Cu失去电子生成铜离子,阴极氢离子得到电子生成氢气,电极总反应为:Cu+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cu2+,故D正确;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握电解原理、电解反应为解答的关键,侧重分析与应用能力的考查,注意离子的放电顺序,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
5.下列关于有机化合物的说法正确的是( )
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 | |
| B. | 戊烷有两种同分异构体 | |
| C. | 乙烯、聚乙烯和苯分子均含有碳碳双键 | |
| D. | 糖类、油脂和蛋白质均可发生水解反应 |
2.常温下,下列溶液可用铁制或铝制容器盛装的是( )
| A. | 浓盐酸 | B. | 浓硝酸 | C. | 稀硫酸 | D. | 稀盐酸 |
9.反应A2+3B2?2AB3以下表示的反应速率中,速率最大的是( )
| A. | υ(A2)=0.4 mol•L-1•min-1 | B. | υ(B2)=1.2 mol•L-1•min-1 | ||
| C. | υ(AB3)=0.6 mol•L-1•min-1 | D. | υ(AB3)=0.9 mol•L-1•min-1 |
19.下列溶液一定呈中性的是( )
| A. | pH=7的溶液 | |
| B. | 加酚酞试液后呈无色的溶液 | |
| C. | c(H+)=c(OH-)=10-6mol/L的溶液 | |
| D. | 由等物质的量的强酸与强碱反应得到的溶液 |
6.25℃时,下列各组离子在指定溶液中可能大量共存的是( )
| A. | pH=l的溶液中:Na+、K+、MnO4-、I- | |
| B. | 无色溶液中:Al3+、NH4+、Cl-、S2- | |
| C. | 由水电离出的c(H+)=1×10 -3 mol•L-1的溶液中:Mg 2+、Cu 2+、SO42-、NO3- | |
| D. | 0.lmol•L-1FeC13溶液中:Fe 2+、NH 4 +、SCN-、SO42- |
3.下列说法正确的是( )
| A. | 活化分子间的碰撞一定发生化学反应 | |
| B. | 吸热反应只有加热才能发生 | |
| C. | 有能量变化的一定是化学反应 | |
| D. | 有化学键断裂不一定发生化学反应 |
8.下列说法正确的是( )
| A. | (CH3CH2)2CHCH3的系统命名为2-乙基丁烷 | |
| B. | 甲酸(HCOOH)和乙二酸(HOOC-COOH)互为同系物 | |
| C. | 有机物CH3-CH2-NO2和H2N-CH2-COOH是同分异构体 | |
| D. | H2与D2互为同位素 |

 .
.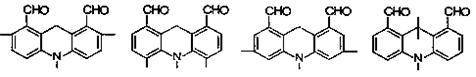 .
. 结构;
结构;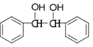 写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)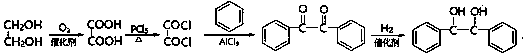 .
.