题目内容
4.化合物F是一种具有强双光子性质的物质,可以通过以下方法合成:
(1)在A、B、C、D、F中的含氧官能团名称为硝基、羰基 .
(2)B→C的反应类型为还原反应.
(3)E的分子是为C14H13N,写出E的结构简式
 .
.(4)写出同时满足下列条件的F的一种同分异构体的结构简式
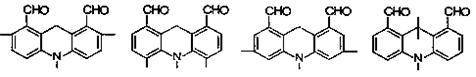 .
.①能发生银镜反应;
②含有
 结构;
结构;③分子中只有6种不同化学环境的氢.
(5)已知:RCOOH$→_{△}^{PCl_{3}}$RCOCl
请以苯和乙二醇为原料制备1,2-二苯基乙二醇
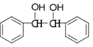 写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)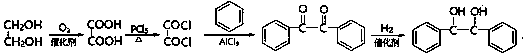 .
.
分析 (1)结合流程图判断出ABCDF中含有的官能团,再确定含有的含氧官能团;
(2)B→C是硝基转化为氨基,是加氢或脱氧反应,由此判断反应类型;
(3)在D→E→F的变化过程中碳架结构不变,碳原子守恒,结合E的分子式推断E的结构简式;
(4)官能团满足的条件为:①能发生银镜反应,说明含有醛基;②含有  结构;③分子中只有6种不同化学环境的氢,说明结构相对对称,由此逐一写出符合条件的同分异构体的结构简式;
结构;③分子中只有6种不同化学环境的氢,说明结构相对对称,由此逐一写出符合条件的同分异构体的结构简式;
(5)以苯和乙二醇为原料制备1,2-二苯基乙二醇 ,可利用乙二醇催化氧化为乙二酸,再根据题中信息在PCl3的作用下生成COClCOCl,再与苯发生取代反应,最后再加氢还原即可.
,可利用乙二醇催化氧化为乙二酸,再根据题中信息在PCl3的作用下生成COClCOCl,再与苯发生取代反应,最后再加氢还原即可.
解答 解:(1)结合流程图中A、B、C、D、F的结构简式可知,在A、B、C、D、F中中的含氧官能团名称为硝基、羰基;故答案为:硝基;羰基;(2)B→C是将硝基还原为氨基,发生的反应类型为还原反应,故答案为:还原反应;
(3)根据D→E的反应物是C2H5Cl与 ,并结合F的结构简式和E的分子式为C14H13N,可知E的结构简式为
,并结合F的结构简式和E的分子式为C14H13N,可知E的结构简式为  ;故答案为
;故答案为 :;
:;
(4)①能发生银镜反应,可知结构中含有醛基;②含有 结构;③分子中只有6种不同化学环境的氢,可知结构具有一定的对称性;则符合条件的F的一种同分异构体的结构简式可能为
结构;③分子中只有6种不同化学环境的氢,可知结构具有一定的对称性;则符合条件的F的一种同分异构体的结构简式可能为  ,
,
故答案为: ;
;
(5)以苯和乙二醇为原料制备1,2-二苯基乙二醇 的合成路线流程图为
的合成路线流程图为 ,
,
故答案为: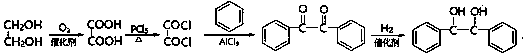 .
.
点评 结合有机合成流程,推断多官能团有机物的结构、性质及符合条件的同分异构体的书写,综合性较强,难点是根据要求设计合成路线,对学生综合利用信息的能力要求较高.

练习册系列答案
相关题目
6.下列制取单质的反应中,化合物作还原剂的是( )
| A. | 用铝和氧化铁在高温下反应制取铁 | B. | 用溴和碘化钾溶液反应制取碘 | ||
| C. | 用碳和高温水蒸汽反应制取氢气 | D. | 用氢气和灼热的氧化铜反应制取铜 |
3.用一定方法可除去下列物质所含的少量杂质(括号内为杂质),其中所加物质能达到除杂目的是( )
| A. | Cl2(HCl)用NaOH溶液 | B. | Na2CO3(NaHCO3)用HCl溶液 | ||
| C. | NaCl溶液(I2)用CCl4 | D. | FeCl2(FeCl3)通入Cl2 |
9.硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7•10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质.以硼镁泥为原料制取的七水硫酸镁在印染、造纸和医药等工业上都有广泛的应用.硼镁泥制取七水硫酸镁的工艺流程如图:

回答下列问题:
(1)Na2B4O7•10H2O中B的化合价为+3.
(2)Na2B4O7易溶于水,也较易发生水解:B4O72-+7H2O?4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小).写出加入硫酸时Na2B4O7发生反应的化学方程式:Na2B4O7+H2SO4+5H2O═Na2SO4+4H3BO3↓.
(3)滤渣B中含有不溶于稀盐酸但能溶于浓盐酸的黑色固体,写出生成黑色固体的离子方程式ClO-+Mn2++H2O═MnO2+Cl-+2H+.
(4)加入MgO的目的是调节溶液的pH值,使Fe3+转化为Fe(OH)3除去.
(5)己知MgSO4、CaSO4的溶解度如表:
操作“A”是将MgSO4和CaSO4混合溶液中的CaS、SO4除去,根据上表数据,简要说明“操作A”步骤为蒸发浓缩,趁热过滤.
(6)Na2B4O7•10H2O失去全部结晶水后的硼砂与金属钠、氢气及石英砂一起反应可制备有机化学中的“万能还原剂--NaBH4”(该过程B的化合价不变).
①写出NaBH4的电子式 .
.
②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力.NaBH4的有效氢含量为0.21(计算结果保留两位小数).
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式BO2-+6H2O+8e-═BH4-+8OH-.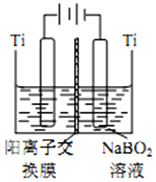

回答下列问题:
(1)Na2B4O7•10H2O中B的化合价为+3.
(2)Na2B4O7易溶于水,也较易发生水解:B4O72-+7H2O?4H3BO3(硼酸)+2OH-,(硼酸在常温下溶解度较小).写出加入硫酸时Na2B4O7发生反应的化学方程式:Na2B4O7+H2SO4+5H2O═Na2SO4+4H3BO3↓.
(3)滤渣B中含有不溶于稀盐酸但能溶于浓盐酸的黑色固体,写出生成黑色固体的离子方程式ClO-+Mn2++H2O═MnO2+Cl-+2H+.
(4)加入MgO的目的是调节溶液的pH值,使Fe3+转化为Fe(OH)3除去.
(5)己知MgSO4、CaSO4的溶解度如表:
| 温度(℃) 溶解度(g) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)Na2B4O7•10H2O失去全部结晶水后的硼砂与金属钠、氢气及石英砂一起反应可制备有机化学中的“万能还原剂--NaBH4”(该过程B的化合价不变).
①写出NaBH4的电子式
 .
.②“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克H2的还原能力.NaBH4的有效氢含量为0.21(计算结果保留两位小数).
③在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式BO2-+6H2O+8e-═BH4-+8OH-.

16.对于1mol/L的NaOH溶液,下列有关说法正确的是(NA表示阿伏加德罗常数)( )
| A. | Na+的数目为NA | B. | OH-的物质的量为1mol | ||
| C. | Na+的物质的量浓度为1mol/L | D. | NaOH的质量为40g |
13.短周期主族元素X、Y、Z在周期表中的位置如图所示.下列说法正确的是( )
| Z | |
| X | Y |
| A. | Z元素的最高正化合价,一定等于其主族序数 | |
| B. | 它们的原子半径由大到小的顺序一定是Y>X>Z | |
| C. | 若它们的原子最外层电子数之和为11,则它们均为非金属元素 | |
| D. | 若它们均为非金属元素,则X与氧元素组成的物质一定是酸性氧化物 |
14.下列离子方程式书写不正确的是( )
| A. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | H2S的电离方程式为 H2S+H2O?HS-+H3O+ | |
| C. | 用铁做电极电解饱和食盐水的阳极反应式:Fe-2e-═Fe2+ | |
| D. | 用两个铜片作电极电解盐酸:Cu+2H+ $\frac{\underline{\;电解\;}}{\;}$H2↑+Cu2+ |

 (1)事实证明,能设计成原电池的反应通常是放热反应.下列化学反应在理论上可以设计成原电池的是B.
(1)事实证明,能设计成原电池的反应通常是放热反应.下列化学反应在理论上可以设计成原电池的是B.