题目内容
在实验室中用MnO2和浓盐酸反应制备纯净干燥的氯气.实验室制取Cl2的原理是:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.以下是一个学生设计的实验装置图.

(1)这个装置中有哪些错误?请分别指出:
① ② ③ ④ ⑤ (有几处填几处)
(2)在改正的装置中:
①洗气瓶中饱和食盐水的作用是 ,浓H2SO4的作用是 .
②烧杯中的NaOH溶液的作用是 .
| ||

(1)这个装置中有哪些错误?请分别指出:
①
(2)在改正的装置中:
①洗气瓶中饱和食盐水的作用是
②烧杯中的NaOH溶液的作用是
考点:氯气的实验室制法
专题:
分析:(1)本题的实验目的是制得纯净、干燥的氯气,用MnO2和浓盐酸共热制得的氯气中,有挥发出来的HCl气体和水蒸气,这是两种要除掉的杂质.用饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气,为达到目的,应先除HCl,后除水蒸气,且洗气装置应长管进、短管出,而图中两个洗气瓶的进出气导管都装反了.另外,本反应的条件是加热,且给烧瓶加热时应垫上石棉网,据此解答.
(2)用饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气;
氯气有毒不能直接排放到空气中,氯气与氢氧化钠反应,可以用氢氧化钠吸收.
(2)用饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气;
氯气有毒不能直接排放到空气中,氯气与氢氧化钠反应,可以用氢氧化钠吸收.
解答:
解:(1)二氧化锰和浓盐酸制取氯气需要加热,圆底烧瓶不能直接加热,洗气装置中导气管遵循“长进短出”原则,装置中应该先除杂后干燥;
故答案为:烧瓶下面缺石棉网;铁圈下面缺酒精灯;盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒;两个洗气瓶中的气体入口导管和出口导管装反了;洗气装置中导气管遵循“长进短出”原则;
(2)①饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气;
故答案为:吸收Cl2中混有的氯化氢气体;吸收Cl2中混有的水蒸气;
②氯气有毒不能直接排放到空气中,氯气与氢氧化钠反应,可以用氢氧化钠吸收,
故答案为:吸收多余的氯气.
故答案为:烧瓶下面缺石棉网;铁圈下面缺酒精灯;盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒;两个洗气瓶中的气体入口导管和出口导管装反了;洗气装置中导气管遵循“长进短出”原则;
(2)①饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气;
故答案为:吸收Cl2中混有的氯化氢气体;吸收Cl2中混有的水蒸气;
②氯气有毒不能直接排放到空气中,氯气与氢氧化钠反应,可以用氢氧化钠吸收,
故答案为:吸收多余的氯气.
点评:本题为实验题,考查了氯气的实验室制法,熟悉实验室制取氯气的反应原理和实验过程是解题关键,注意除杂的顺序,题目难度不大.

练习册系列答案
相关题目
 某同学在研究元素周期表中前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中O点代表氢元素.下列说法中不正确的是( )
某同学在研究元素周期表中前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中O点代表氢元素.下列说法中不正确的是( )| A、离O点越远的元素,其原子半径越大 |
| B、虚线相连的元素处于同一族 |
| C、B元素是图中金属性最强的元素 |
| D、由元素A、B组成的化合物中可能含有共价键 |
下列各组物质的熔、沸点高低只与范德华力有关的是( )
| A、Li、Na、K、Pb |
| B、HF、HCl、HBr、HI |
| C、LiCl、NaCl、KCl、RbCl |
| D、F2、Cl2、Br2、I2 |
已知AgI为黄色沉淀,AgCl为白色沉淀.25℃时,AgI饱和溶液中c(Ag+)=1.22×10-8 mol?L-1 ,AgCl饱和溶液中c(Ag+)=1.30×10-5mol?L-1.若在5mL含有KCl和KI浓度均为0.01mol?L-1的混合溶液中,滴加8mL 0.01mol?L-1的AgNO3溶液,则下列叙述中不正确的是( )
| A、溶液中所含溶质的离子浓度大小关系为:c(NO3-)>c(K+)>c(Cl-)>c(I-)>c(Ag+) |
| B、溶液中先产生的是AgI沉淀 |
| C、AgCl的KSP的数值为1.69×10-10 |
| D、若在AgI悬浊液中滴加KCl溶液,黄色沉淀可能转变成白色沉淀 |
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是( )
A、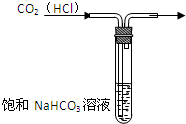 除去混有的杂质气体 |
B、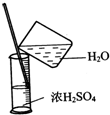 浓硫酸稀释 |
C、 分离出AgNO3溶液中的AgCl |
D、 称量30.46g的NaOH固体 |
某同学在实验报告中记录下列数据,其中正确的是( )
| A、第一节用25mL量筒量取12.36mL盐酸 |
| B、第二节用托盘天平称量8.75g食盐 |
| C、第三节用500mL的容量瓶配制450mL溶液 |
| D、第四节用广泛pH试纸测得某溶液的pH为3.5 |
随着核电荷数的增大,下列关于碳族元素的性质递变说法错误的是( )
| A、元素的原子半径逐渐增大 |
| B、元素的原子失电子能力逐渐增强 |
| C、元素的金属性逐渐增强 |
| D、元素最高价氧化物的水化物的酸性逐渐增强 |