题目内容
1.为了除去氯化钾中含有的少量硫酸镁和氯化钙杂质,需进行下列六项操作:①加水溶解 ②加热蒸发得到晶体 ③加入过量的氢氧化钡溶液 ④加入适量的盐酸 ⑤加入过量碳酸钾 ⑥过滤,先后次序正确的是( )| A. | ①④③⑤⑥② | B. | ①⑤③④⑥② | C. | ①③④⑥⑤② | D. | ①③⑤⑥④② |
分析 除去氯化钾中含有的少量硫酸镁和氯化钙杂质,选择碱除去镁离子,选择碳酸钾除去钙离子,最后加盐酸,以此来解答.
解答 解:除去氯化钾中含有的少量硫酸镁和氯化钙杂质,镁离子用过量的氢氧化溶液除去,钙离子用过量的碳酸钾溶液除去,同时可以除去过量的钡离子,过滤后,然后过量的氢氧根离子及碳酸根离子用适量的盐酸除去,蒸发溶液可得氯化钾固体,所以正确的顺序是①③⑤⑥④②,
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及试剂的加入顺序等为解答的关键,侧重分析与实验能力的考查,注意碳酸钾一定在氢氧化钡之后,题目难度不大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
11.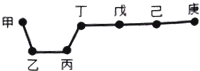 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素.下列判断正确的是( )| A. | 甲与己形成的化合物一定是离子化合物 | |
| B. | 简单气态氢化物的稳定性:庚>己>戊 | |
| C. | 乙、丙、丁的最高价氧化物水化物可以相互反应 | |
| D. | 庚的最高价氧化物水化物酸性最强 |
12.运用化学知识,判断下列与安全有关的问题,其中不正确的是( )
| A. | 氢气与氯气应分别贮存在钢瓶中,并放在同一安全室集中保存 | |
| B. | 电石、Na2O2着火时,不能用常规的水枪灭火 | |
| C. | 可燃性颗粒(如面粉,漆粉)弥漫到空气中,可能会引起爆炸 | |
| D. | 油锅着火可用金属锅盖盖灭 |
16.下列实验操作、现象、结论或解释均正确的是( )
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 将某钾盐固体溶于盐酸 | 产生无色无味的气体 | 该钾盐是K2CO3 |
| B | 向可能含有Fe2+的Fe2(SO4)3溶液中加入酸性KMnO4溶液 | KMnO4溶液褪色 | 该溶液中一定含有Fe2+ |
| C | 向某溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| D | 向浓度均为0.1 mol•L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
6.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1的氯化铁溶液中,若Fe3+的数目为 NA,则Cl-的数目为3NA | |
| B. | 常温下,1 mol Fe与足量稀HNO3反应,转移电子的数目为2 NA | |
| C. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| D. | 标准状况下,2.24 LCl2溶于水,转移电子的数目为0.1NA |
13.化学与社会、科学、技术、环境等有密切关系.下列说法正确的是( )
| A. | 硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果 | |
| B. | 含乙醇、NaClO、H2O2等消毒液均可以将病毒氧化而达到消毒目的 | |
| C. | 有机玻璃受热软化,易于加工成型,是一种硅酸盐材料 | |
| D. | 处理废水时,加入明矾作为消毒剂除去水中的细菌 |
4.三氯化磷分子和氨分子结构和空间构型相似,是三角锥形而不是平面正三角形,下列关于三氯化磷分子的叙述,不正确的是( )
| A. | PCl3分子中三个共价键的键长、键能和键角都相等 | |
| B. | PCl3分子中的P-Cl 键属于极性共价键 | |
| C. | PCl3分子中既有σ键,又有π键 | |
| D. | PCl3分子中各原子都达到8电子稳定结构 |
 .
. .
.