题目内容
下列物质不能使品红溶液褪色的是( )
| A、Cl2 |
| B、NH3 |
| C、Na2O2 |
| D、SO2 |
考点:氯气的化学性质,重要的还原剂,二氧化硫的化学性质
专题:卤族元素,氮族元素
分析:HClO、Na2O2、臭氧都具有强氧化性而使品红溶液褪色,SO2能和有色物质反应生成无色物质而具有漂白性,据此分析解答.
解答:
解:HClO、Na2O2、臭氧都具有强氧化性而使品红溶液褪色,氯气和水反应生成的HClO能漂白品红试液,SO2能和有色物质反应生成无色物质而具有漂白性,所以SO2也能漂白品红溶液,氨气没有漂白性,不能漂白品红溶液,故选B.
点评:本题考查物质的漂白性,侧重考查元素化合物知识,知道HClO、Na2O2、臭氧、活性炭、SO2等物质漂白原理,注意SO2不能漂白酸碱指示剂,题目难度不大.

练习册系列答案
相关题目
下列反应中,不属于四种基本反应类型,但属于氧化还原反应的是( )
| A、CH4+2O2═CO2+2H2O | ||||
| B、2Na+2H2O=2NaOH+H2↑ | ||||
C、2KClO3
| ||||
| D、CaCO3+2HCl=CaCl2+H2O+CO2↑ |
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法不正确的是( )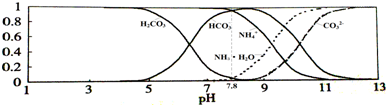

| A、NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3?H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| B、往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 |
| C、通过分析可知常温下Kb(NH3?H2O)>Ka1(H2CO3) |
| D、当溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3?H2O)>c(CO32-) |
下列物质中,只含离子键的是( )
| A、N2 |
| B、HCl |
| C、MgCl2 |
| D、KOH |
在MgCl2、Cl2、Ca(ClO)2、HClO2、( )、Cl2O7的排列中,括号内应填入的物质的化学式是( )
| A、KClO4 |
| B、KClO3 |
| C、HClO |
| D、Cl2O3 |


