题目内容
写出下列反应的离子方程式
(1)硫酸铜溶液与氢氧化钠溶液混合
(2)碳酸钠溶液与稀盐酸混合
(3)氢氧化钡溶液与稀硫酸混合
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应 .
(1)硫酸铜溶液与氢氧化钠溶液混合
(2)碳酸钠溶液与稀盐酸混合
(3)氢氧化钡溶液与稀硫酸混合
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应
考点:离子方程式的书写
专题:
分析:(1)硫酸铜溶液与氢氧化钠溶液混合反应生成氢氧化铜和硫酸钠;
(2)碳酸钠溶液与稀盐酸混合反应生成氯化钠和水、二氧化碳;
(3)氢氧化钡溶液与稀硫酸反应生成硫酸钡和水;
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应生成碳酸钙、氢氧化钠和水.
(2)碳酸钠溶液与稀盐酸混合反应生成氯化钠和水、二氧化碳;
(3)氢氧化钡溶液与稀硫酸反应生成硫酸钡和水;
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应生成碳酸钙、氢氧化钠和水.
解答:
解:(1)硫酸铜溶液与氢氧化钠溶液混合反应生成氢氧化铜和硫酸钠,离子方程式为:Cu2++2OH-═Cu(OH)2↓;
故答案为:Cu2++2OH-═Cu(OH)2↓;
(2)碳酸钠溶液与稀盐酸混合离子方程式为:CO32-+2H+=H2O+CO2↑;
故答案为:CO32-+2H+=H2O+CO2↑;
(3)氢氧化钡溶液与稀硫酸混合,离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
故答案为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应,离子方程式为:Ca2++OH-+HCO3-=CaCO3↓+H2O;
故答案为:Ca2++OH-+HCO3-=CaCO3↓+H2O.
故答案为:Cu2++2OH-═Cu(OH)2↓;
(2)碳酸钠溶液与稀盐酸混合离子方程式为:CO32-+2H+=H2O+CO2↑;
故答案为:CO32-+2H+=H2O+CO2↑;
(3)氢氧化钡溶液与稀硫酸混合,离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
故答案为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O;
(4)少量的碳酸氢钠溶液与过量的澄清石灰反应,离子方程式为:Ca2++OH-+HCO3-=CaCO3↓+H2O;
故答案为:Ca2++OH-+HCO3-=CaCO3↓+H2O.
点评:本题考查了离子方程式的书写,明确离子方程式书写的方法和反应的实质是解题关键,题目难度不大.

练习册系列答案
相关题目
下列数量的各物质所含原子个数由大到小顺序排列的是( )
①0.5mol氨气 ②1g氢气 ③4℃时9mL水④0.2mol磷酸钠.
①0.5mol氨气 ②1g氢气 ③4℃时9mL水④0.2mol磷酸钠.
| A、④③②① | B、①④③② |
| C、②③④① | D、①④②③ |
下列各溶液中,Na+ 浓度最大的是( )
| A、1 L 1.2 mol?L-1的NaCl溶液 |
| B、2 L 1 mol?L-1的NaOH溶液 |
| C、0.5 L 0.8 mol?L-1的Na2SO4溶液 |
| D、3 L 0.5 mol?L-1的Na2CO3溶液 |
下列化学方程式中,不能用离子方程式H++OH-═H2O表示的是( )
| A、2NaOH+H2SO4═Na2SO4+2H2O |
| B、Ba(OH)2+2HCl═BaCl2+2H2O |
| C、HCl+KOH═KCl+H2O |
| D、Cu(OH)2+2HNO3═Cu(NO3)2+2H2O |
下列实验装置选择正确,能达到目的是( )
A、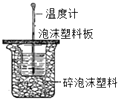 测定酸碱反应中和热 |
B、 测定反应速率 |
C、 实现化学能转换为电能 |
D、 测定食醋浓度 |
牙齿表面覆盖的牙釉质是人体中最坚硬的部分,起着保护牙齿的作用,其主要成分为羟基磷酸钙[Ca5(PO4)3OH].在牙齿表面存在着如下平衡:Ca5(PO4)3OH(s)?5Ca2+(aq)+3PO43-(aq)+OH-(aq) Ksp=6.8×10-37.下列说法错误的是( )
| A、残留在牙齿上的糖发酵会产生H+,经常吃糖易造成龋齿 |
| B、由上述平衡可知,小孩长牙时要少吃糖多补钙 |
| C、若减小OH-的浓度,上述平衡将向右移动,Ksp的值相应增大 |
| D、使用含氟牙膏能防止龋齿,是因为Ca5(PO4)3OH(s)转化为更难溶的Ca5(PO4)3F(s)[Ca5(PO4)3F(s)的Ksp=2.8×10-61] |
某溶液中有Fe3+、Mg2+、Fe2+和Na+四种离子,向其中加入过量的氢氧化钠溶液并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是( )
| A、Fe3+ |
| B、Mg2+ |
| C、Fe2+ |
| D、Na+ |