题目内容
下列实验装置选择正确,能达到目的是( )
A、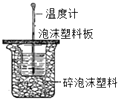 测定酸碱反应中和热 |
B、 测定反应速率 |
C、 实现化学能转换为电能 |
D、 测定食醋浓度 |
考点:化学实验方案的评价
专题:实验设计题
分析:A.测定中和热时,为充分反应,应搅拌;
B.气体从长颈漏斗逸出;
C.根据原电池的组成判断;
D.应用碱式滴定管.
B.气体从长颈漏斗逸出;
C.根据原电池的组成判断;
D.应用碱式滴定管.
解答:
解:A.测定中和热时,为充分反应,应用环形玻璃棒搅拌,故A错误;
B.气体从长颈漏斗逸出,应用分液漏斗,故B错误;
C.锌为负极,铜为正极,能进行自发进行的氧化还原反应,可形成原电池,故C正确;
D.氢氧化钠可腐蚀玻璃,应用碱式滴定管,故D错误.
故选C.
B.气体从长颈漏斗逸出,应用分液漏斗,故B错误;
C.锌为负极,铜为正极,能进行自发进行的氧化还原反应,可形成原电池,故C正确;
D.氢氧化钠可腐蚀玻璃,应用碱式滴定管,故D错误.
故选C.
点评:本题考查较为综合,涉及中和热的测定、原电池以及中和滴定等,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度中等.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A、生成40.0LN2(标准状况) |
| B、有0.250molKNO3被氧化 |
| C、转移电子的物质的量为1.25mol |
| D、被氧化的N原子的物质的量为3.5mol |
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+.下列说法不正确的是( )
| A、H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B、在H2O2分解过程中,溶液的酸碱性不变 |
| C、在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| D、H2O2生产过程要严格避免混入Fe2+ |
有机化学是化学学科的重要分支,在卫生、医药、农业、材料、国防等领域发挥着越来越重要的作用.请判断,下列各项中不属于有机化学研究范围的是( )
| A、合成自然界中不存在,但对人类有用的有机化合物 |
| B、制造半导体材料--芯片(Si) |
| C、破译蛋白质组成密码,认识并改造遗传分子 |
| D、发明不会长期存留、专一性更强的农用化学品,开发安全的食品添加剂 |
下列说法正确的是( )
| A、过滤可使硬水软化 |
| B、硬水经煮沸后就变为软水 |
| C、水垢的主要成分是碳酸氢钙和碳酸氢镁 |
| D、永久硬度是指钙镁类硫酸盐和氯化物引起的水的硬度 |
已知某有机物X的结构简式如图,下列有关叙述不正确的是( )


| A、1molX分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3mol、2mol、1mol |
| B、X在一定条件下能与FeCl3溶液发生显色反应 |
| C、1molX可消耗2molBr2 |
| D、该物质能使酸性高锰酸钾溶液褪色 |


