题目内容
17.下列比较不正确的是( )| A. | 稳定性:HF>HCl>HBr>HI | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性:H2SO4>H3PO4>HClO4 | D. | 氧化性:O2>S>Se |
分析 A.非金属性越强,对应氢化物的稳定性越强;
B.金属性越强,最高价氧化物对应水合物的碱性越强;
C.非金属性越强,最高价氧化物对应水合物的酸性越强;
D.一般情况下,同一主族中元素原子序数越大,非金属性越弱,单质氧化性越弱.
解答 解:A.卤素的原子序数越大,非金属性越弱,对应氢化物的稳定性越弱,则氢化物稳定性大小为:HF>HCl>HBr>HI,故A正确;
B.碱金属元素的原子序数越大,金属性越弱,最高价氧化物对应水合物的碱性越弱,则碱性:NaOH>Mg(OH)2>Al(OH)3,故B正确;
C.非金属性:P<S<Cl,最高价氧化物对应水合物的酸性:HClO4>H2SO4>H3PO4,故C错误;
D.氧族元素中,随着原子序数递增,元素氧化性逐渐减弱,则氧化性:O2>S>Se,故D正确;
故选C.
点评 本题考查了原子结构与元素周期律的应用,题目难度中等,明确原子结构与元素周期律的关系为解答关键,注意掌握元素周期律内容、元素周期表结构,试题培养了学生的灵活应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.工业上可用下列装置测定黄铁矿(主要成分为FeS2)中硫的质量分数(忽略SO2、H2SO3与氧气的反应)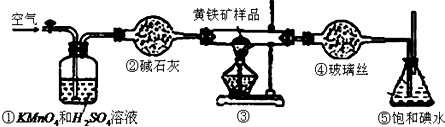
实验的正确操作步骤如下:
A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0g样品小心地放入硬质玻璃管中
D.以1L/min的速率鼓入空气
E.将硬质玻璃管中的黄硫铁矿样品加热到800℃~850℃
F.用300mL的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O═2HI+H2SO4
G.吸收液用CCl4萃取
H.取20.00mL吸收液,用标准0.2000mol•L-1的NaOH溶液滴定.
试回答:
(1)写出装置③中发生反应的化学方程式4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2.
(2)步骤G中所用主要仪器是分液漏斗,应取上(填“上”或“下”)层溶液进行后续实验.
(3)装置①的作用是除去空气中的还原性气体,提高实验的准确率.
(4)装置④的作用是过滤二氧化硫气体避免氧化铁颗粒进入,得到平缓的二氧化硫气流.
(5)步骤H中滴定时应选用酚酞作指示剂,可以根据滴入最后一滴NaOH溶液后,溶液变为浅红色,并在半分钟内不褪色现象来判断滴定已经达到终点.
(6)假定黄硫铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收.滴定得到的数据如表所示:
则硫铁矿样品中硫元素的质量分数为24.0%(保留小数点后1位).
(7)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置⑤所得吸收液中加入下列哪种试剂B.
A.硝酸银溶液 B.氯化钡溶液
C.澄清石灰水 D.酸性高锰酸钾溶液.

实验的正确操作步骤如下:
A.连接好装置,并检查装置的气密性
B.称取研细的黄铁矿样品
C.将2.0g样品小心地放入硬质玻璃管中
D.以1L/min的速率鼓入空气
E.将硬质玻璃管中的黄硫铁矿样品加热到800℃~850℃
F.用300mL的饱和碘水吸收SO2,发生的反应是:I2+SO2+2H2O═2HI+H2SO4
G.吸收液用CCl4萃取
H.取20.00mL吸收液,用标准0.2000mol•L-1的NaOH溶液滴定.
试回答:
(1)写出装置③中发生反应的化学方程式4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2.
(2)步骤G中所用主要仪器是分液漏斗,应取上(填“上”或“下”)层溶液进行后续实验.
(3)装置①的作用是除去空气中的还原性气体,提高实验的准确率.
(4)装置④的作用是过滤二氧化硫气体避免氧化铁颗粒进入,得到平缓的二氧化硫气流.
(5)步骤H中滴定时应选用酚酞作指示剂,可以根据滴入最后一滴NaOH溶液后,溶液变为浅红色,并在半分钟内不褪色现象来判断滴定已经达到终点.
(6)假定黄硫铁矿中的硫在操作E中已全部转化为SO2,并且被饱和碘水完全吸收.滴定得到的数据如表所示:
| 滴定次数 | 待测液体的体积/mL | 标准碱溶液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 第一次 | 20.00mL | 0.00 | 20.98 |
| 第二次 | 20.00mL | 0.22 | 20.20 |
| 第三次 | 20.00mL | 0.36 | 20.38 |
(7)也有人提出用“沉淀质量法”测定黄铁矿中含硫质量分数,若用这种方法测定,最好是在装置⑤所得吸收液中加入下列哪种试剂B.
A.硝酸银溶液 B.氯化钡溶液
C.澄清石灰水 D.酸性高锰酸钾溶液.
12.NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的正戊烷完全燃烧需要氧气分子数为4NA | |
| B. | 标准状况下,22.4L乙烷中所含电子对数目为6NA | |
| C. | 26g乙炔和苯的混合物,含有原子总数为4NA | |
| D. | 标准状况下,22.4L甲烷与氯气光照取代发生一氯取代,需要氯气0.5NA |
2.下列说法错误的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、H+和H2是氢元素的五种不同粒子 | |
| B. | 石墨和金刚石互为同位素,化学性质相似 | |
| C. | ${\;}_{1}^{1}$H和 ${\;}_{1}^{2}$H是不同的核素 | |
| D. | 12C和 14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
6.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题:
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其M电子层的电子数为17.
(2)VSEPR理论认为价层电子对间互斥力(F)大小顺序:F(孤电子对间)>F(孤电子对-成键电子对)>F(成键电子对间),已知XeF4中Xe价层电子对数为6,其VSEPR模型为八面体,为使得价层电子对间的孤电子对斥力最小,预测XeF4分子中的键角应为90°.
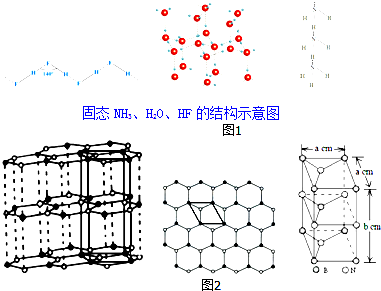
(3)除NH3、H2O、HF外,同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大,沸点越高;
已知NH3、H2O、HF的氢键键能和结构如表:
则如图1H2O、HF、NH3沸点由高到低的顺序依次为:H2O>HF>NH3.
(4)石墨型BN呈白色,亦称“白石墨”.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”中B和N的杂化方式分别为sp2和sp2,白石墨的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3( 已知相对原子质量B:11 N:14 阿伏加德罗常数的数值用NA表示).
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其M电子层的电子数为17.
(2)VSEPR理论认为价层电子对间互斥力(F)大小顺序:F(孤电子对间)>F(孤电子对-成键电子对)>F(成键电子对间),已知XeF4中Xe价层电子对数为6,其VSEPR模型为八面体,为使得价层电子对间的孤电子对斥力最小,预测XeF4分子中的键角应为90°.
(3)除NH3、H2O、HF外,同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大,沸点越高;
已知NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能/kJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |

(4)石墨型BN呈白色,亦称“白石墨”.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”中B和N的杂化方式分别为sp2和sp2,白石墨的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3( 已知相对原子质量B:11 N:14 阿伏加德罗常数的数值用NA表示).
7.胶体是一种微粒直径在1-100nm之间的分散系.下列事实与胶体的性质无关的是( )
| A. | 清晨在密林中看到一缕缕光束 | |
| B. | 盐酸与硝酸银溶液反应生成白色沉淀 | |
| C. | 豆浆中加入盐卤做豆腐 | |
| D. | 一束平行光射入蛋白质溶液中,侧面可看到一束光亮的通路 |
 ;MgF2
;MgF2 .
.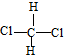 和
和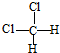
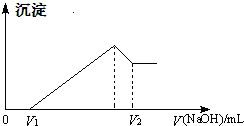 将镁、铝的混合物7.5g溶于100mL 4mol/L的H2SO4溶液中,然后再滴加1mol/L的NaOH溶液.请回答:
将镁、铝的混合物7.5g溶于100mL 4mol/L的H2SO4溶液中,然后再滴加1mol/L的NaOH溶液.请回答: