题目内容
16.碳、硅元素的单质及其化合物是构成自然界的重要物质.(1)甲烷是最简单的有机物,实验室可通过下列反应制取:
CH3COONa+NaOH$→_{△}^{CaO(或MgO)}$CH4↑+X(已配平)
①X属于离子晶体(填晶体类型);
②MgO晶体的熔点比CaO高,主要原因是Mg2+半径比Ca2+小,因此MgO晶体的晶格能较大,熔点较高.
(2)C60、金刚石和石墨是三种重要的碳单质,结构模型分别如图所示(其中石墨仅表示出其中的一层结构).
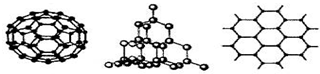
①金刚石中碳原子的杂化方式为sp3;
②石墨层状结构中,平均每个正六边形占有的C-C键数是3个.
分析 (1)①根据原子守恒判断X物质,根据X的构成微粒确定其晶体类型;
②相同类型的离子晶体中,晶体的熔点与晶格能成正比,晶格能与离子半径成反比;
(2)①根据价层电子对互斥理论确定其杂化类型;
②利用均摊法计算.
解答 解:(1)①根据元素守恒及原子守恒知,X是碳酸钠,碳酸钠是由阴阳离子构成的离子晶体;
故答案为:离子;
②MgO晶体的熔点比CaO高都属于离子晶体,Mg2+半径比Ca2+小,键能较大,所以氧化镁晶体的晶格能大于氧化钙,导致氧化镁晶体的熔点大于氧化钙,故答案为:Mg2+半径比Ca2+小,因此MgO晶体的晶格能较大,熔点较高;
(2)①金刚石中每个碳原子和4个碳原子以σ键相结合,且没有孤对电子,所以每个碳原子的价层电子对是4,则碳原子采取sp3杂化,
故答案为:sp3;
②石墨层状结构中,每个碳原子被三个正六边形共用,所以平均每个正六边形占有的碳原子数=6×$\frac{1}{2}$3;
故答案为:3.
点评 本题考查离子晶体的性质,原子的杂化方式和均摊法,注意晶格能的大小比较以及利用均摊法计算晶胞中各种原子个数是难点,题目难度大.

练习册系列答案
相关题目
6.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 25℃、101kPa下,64g SO2中含有的原子数为3NA | |
| C. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
7.下列排序不正确的是( )
| A. | 单质的熔点:钾<铷<铯 | B. | 离子半径:S2->Na+>Mg2+ | ||
| C. | 热稳定性:HF>H2O>H2S | D. | 酸性:H2SiO3<H3PO4<H2SO4 |
4.下列说法不正确的是( )
| A. | 高吸水性树脂属于功能高分子材料 | |
| B. | 食品包装袋、食物保鲜膜等材料的主要成份是聚乙烯 | |
| C. | 人造纤维、合成纤维和光导纤维都是有机高分子化合物 | |
| D. | 高分子化合物的结构大致可以分为线型结构、支链型结构和网状结构三类 |
11.下列离子中外层d轨道达半充满状态的是( )
| A. | 24Cr3+ | B. | 26Fe3+ | C. | 27Co3+ | D. | 29Cu+ |
1.下列文字表述与反应方程式对应且正确的是( )
| A. | 溴苯中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| B. | 利用腐蚀法制作印刷线路板:2Fe3++Cu═2Fe+Cu2+ | |
| C. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 实验室用液溴和苯在催化剂作用下制溴苯: |
8.下列关于使用托盘天平的叙述不正确的是 ( )
| A. | 称量前先调节托盘天平的零点 | |
| B. | 称量时左盘放被称量物,右盘放砝码 | |
| C. | 潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量.其他固体药品可直接放在天平托盘上称量 | |
| D. | 用托盘天平可以准确称量药品0.01g | |
| E. | 称量完毕应把砝码放回砝码盒中 |
15.铜锈是一种绿色化合物,它的成分为碱式碳酸铜,兼有氢氧化铜和碳酸铜的性质.试推测:铜锈在高温灼烧条件下充分反应后的固体物质是( )
| A. | 黑色的氧化铜 | B. | 红色的氧化亚铜 | ||
| C. | 蓝色的氢氧化铜和碳酸铜 | D. | 黑色的氧化亚铜 |
16.为鉴别乙醇、乙酸、葡萄糖溶液,选用一种试剂,可为下列中的( )
| A. | 氢氧化钠 | B. | 硝酸 | C. | 碘 | D. | 新制氢氧化铜 |