题目内容
18.下列各组物质均属于分子晶体且均为化合物的是( )| A. | NH3、HD、C10H8 | B. | PCl3、CO2、AlCl3 | C. | SO2、SiO2、P2O5 | D. | CCl4、H2O2、Na2S |
分析 化合物由两种或两种以上的元素组成的纯净物;通过分子间作用力互相结合形成的晶体叫做分子晶体.如:所有的非金属氢化物,大多数的非金属氧化物,绝大多数的共价化合物,少数盐(如AlCl3).
解答 解:A.HD是氢气分子,属于单质,故A错误;B.PCl3、CO2、AlCl3均是分子晶体,且均是化合物,故B正确;C.SiO2是二氧化硅晶体的化学式,不是分子式,是由共价键形成的原子晶体,故C错误;D.硫化钠是由钠离子和硫离子形成的离子晶体,故D错误,故选B.
点评 本题考查晶体类型的判断,难度不大.注意把握晶体的构成粒子以及常见物质的晶体类型.

练习册系列答案
相关题目
12.下列反应属于放热反应的是( )
| A. | 破坏生成物全部化学键所需能量小于破坏反应物全部化学键所需能量 | |
| B. | HCO3-+H2O?CO32-+H3O+ | |
| C. | HCO3-+H2O?H2CO3+OH- | |
| D. | CH3COOH+KOH?CH3COOK+H2O |
9.下列实验操作不能达到实验目的是( )
| A. | 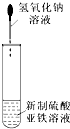 可以制备Fe(OH)2并可以较长时间观察到Fe(OH)2的颜色 | |
| B. | 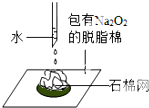 可以证明过氧化钠与水反应是放热反应 | |
| C. | 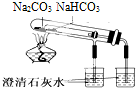 可以证明碳酸钠热稳定性比碳酸氢钠好 | |
| D. | 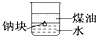 可以证明密度:ρ(煤油)<ρ(钠)<ρ(水) |
6.NA表示阿伏加德罗常数.下列说法正确的是( )
| A. | 标准状态下,33.6 L氟化氢中含有1.5 NA个氟化氢分子 | |
| B. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| C. | 1molNaCl晶体中含有NA个Na+ | |
| D. | 28g乙烯分子中含有极性共价键的数目为6NA |
13.下列说法正确的是( )
| A. | 有机物CH3C(CH3)3的系统命名为2,2-二甲基新戊烷 | |
| B. | 樱桃是一种抗氧化的水果,樱桃中含有一种羟基酸,如图所示 ,通常条件下,该羟基酸可以发生取代、氧化和加成反应 ,通常条件下,该羟基酸可以发生取代、氧化和加成反应 | |
| C. | 涤纶是由对苯二甲酸(PTA)和乙二醇(EG)通过加聚反应得到的 | |
| D. | 等质量的甲醛和乙酸充分燃烧耗氧量相同 |
3.下列各组离子能够大量共存且溶液呈无色的是( )
| A. | K+、Na+、Cl-、CO32- | B. | Mg2+、Al3+、OH-、SO42- | ||
| C. | H+、Ag+、Cl-、SO42- | D. | Fe2+、H+、Na+、NO3- |
10.下列图示的四种实验操作名称从左到右依次是( )
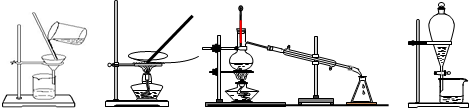

| A. | 过滤、蒸发、蒸馏、萃取分液 | B. | 过滤、蒸馏、蒸发、萃取分液 | ||
| C. | 蒸发、蒸馏、过滤、萃取分液 | D. | 萃取分液、蒸馏、蒸发、过滤 |
7.下列离子方程式正确的是( )
| A. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| B. | 硫氢化钠的水解:HS-+H2O?H3O++S2- | |
| C. | 不断加热煮沸氯化铁溶液:Fe3++3H2O?Fe(OH)3+3H+ | |
| D. | NH4Cl水解:NH4++H2O?NH3•H2O+H+ |
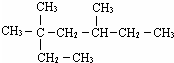 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷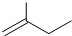 C5H10.
C5H10.