题目内容
将标准状况下22.4L的HCl溶于水配成200mL的溶液,所得溶液的物质的量浓度为 mol/L;配制300mL0.5mol?L-1氯化钠溶液,需要1.5mol?L-1的氯化钠溶液的体积是 mL.
考点:物质的量浓度的相关计算
专题:计算题
分析:结合n=
、c=
及配制溶液前后溶质的物质的量不变来计算.
| V |
| Vm |
| n |
| V |
解答:
解:标准状况下22.4L的HCl溶于水配成200mL的溶液,所得溶液的物质的量浓度为
=5mol/L;
配制溶液前后溶质的物质的量不变,则配制300mL0.5mol?L-1氯化钠溶液,需要1.5mol?L-1的氯化钠溶液的体积为
=0.1L=100mL,
故答案为:5;100.
| ||
| 0.2L |
配制溶液前后溶质的物质的量不变,则配制300mL0.5mol?L-1氯化钠溶液,需要1.5mol?L-1的氯化钠溶液的体积为
| 0.3L×0.5mol/L |
| 1.5mol/L |
故答案为:5;100.
点评:本题考查物质的量浓度的相关计算,为高频考点,把握物质的量、浓度、体积之间的关系及配制溶液的计算等为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
有关下列图象的说法正确的是( )
A、 表示的反应速率随温度变化的关系可知该反应的△H>0 |
B、 表示向pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,则其中曲线a对应的是醋酸 |
C、 表示该反应为放热反应.且催化剂能降低反应的活化能、改变反应的焓变 |
D、 中开关K置于a或b处均可减缓铁的腐蚀 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O△H<0,在恒容的密闭容器中,下列有关说法正确的是( )
| 催化剂 |
| 180℃ |
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数减小 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、单位时间内消耗NO和N2的物质的量比为1:2时,反应没有达到平衡 |
| D、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
下列说法正确的是( )
A、已知1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化如图1,则NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=+234kJ/mol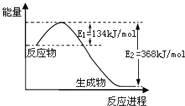 | ||||||||
B、一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| ||||||||
| C、已知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液浓度为 5.6×10-5 mol/L,则生成沉淀所需Na2CO3溶液最小浓度为 5×10-5 mol/L | ||||||||
D、在不同条件下进行的异构化反应 X?Y 的进程图解如下.图2中的“ ”是X,“ ”是X,“ ”是Y,则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小 ”是Y,则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小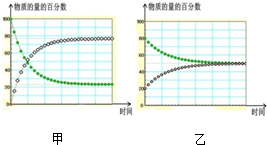 |
欲将蛋白质从水析出而又不改变它的性质,应加入( )
| A、酒精溶液 |
| B、Na2SO4溶液 |
| C、Pb(NO3)2溶液 |
| D、NaOH溶液 |

 用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):